
УДК 662 ББК 35.63
П 33

Составитель серии Л. Делла-Росса
Оформление серии Г. Калашников
Серия основана в 2004 году
Платов Г. А.
П 33 Пиротехник. Искусство изготовления фейерверков. — М.г Изд-во Книжкин Дом, Изд-во Эксмо, 2004. — 320 с. — * (Экспресс-курс).
ISBN 5-699-08586-6
Пиротехника как искусство начала зарождаться в те времена, когда, замирая от ужаса и восхищения, древние люди смотрели на искры, летящие из костра. В современном мире огонь не утратил своего очарования. Любой из нас любовался зрелищем фейерверка или салюта, однако такое чудо, к сожалению, не происходит ежедневно. Конечно, мы могли бы устроить фейерверк к какому-либо торжеству самостоятельно, приобретя уже готовые изделия, но то, что предлагают нам продавцы, во-первых, дорого, а во-вторых, далеко не безопасно.
Мы предлагаем вниманию читателей уникальную книгу, в которой собраны поистине бесценные технологии и рецептуры изготовления пиротехнических средств, начиная от простых бенгальских огней и закан -чивая разноцветными салютами и фейерверками. Самое удивительное, что ВСЕ, о чем рассказано в книге, можно изготовить своими руками, без всякого вреда для здоровья (при условии соблюдения правил техники безопасности!) и из компонентов, которые легко можно приобрести в магазинах или аптеках.
УДК 662
. ББК 35.63
ISBN 5-699-08586-6
© Платов Г. А., 2004
© Обложка. Калинченко Ю., 2004
© Оригинал-макет.
ООО «Издательство «Книжкин Дом», 2004 © Издание. ООО «Издательство «Эксмо», 2004
Родился в 1934 году. С 1950 года работал на киностудии «Мосфильм», в оружейно-пиротехническом цехе с 1957 по 2001 год — год ухода на отдых. С 1996 года — заместитель начальника цеха, технорук. С 1999 года — технолог, должность заместителя начальника.цеха упразднили.
За время работы подал несколько заявок, рационализаторских предложений. На некоторые из них (23 шт.) имеются свидетельства.
Разрабатывал и применял на съемках различные эффекты. Принимал участие в съемках кинокартин, а в некоторых руководил бригадами пиротехников: «Баллада о солдате», «Железный поток», «Сашка», «Битва за Москву», «У твоего порога», «Холодное лето 53 года», «Тегеран-43» (впервые сделал эффект попадания пули в лицо человека — А. Джигарханян), «Сталинград», «Закон» и др.

__________ ПИРОТЕХНИК
До девяностых годов прошлого века пиротехнический цех «Мосфильма» был законодателем и монополистом по производству фейерверков на всей территории СССР. Даже в середине девяностых годов, когда сжигателей фейерверков, изготовленных в ЮВА (ЮВА — Юго-Восточная Азия: Китай, Вьетнам, Бирма, Сингапур, Северная и Южная Кореи), появилось большое количество, на фестивале фейерверков в Московском парке им. Горького нам было присуждено первое место. Мы использовали только собственные материалы и изделия. Сценарий фейерверка также был разработан нами.
До восьмидесятых годов я участвовал во всех семинарах пиротехников, как всесоюзных, так и международных, демократических стран. В 1986 году был приглашен на Кубу для подготовки пиротехников. Провел шестимесячные курсы, где разработал программу, включавшую и взрывные работы.
При ВГИКе дважды организовывались курсы повышения квалификации пиротехников Советского Союза. В последующие годы при «Мосфильме» несколько раз были организованы курсы подготовки молодых пиротехников. За это время при моем участии было подготовлено около тридцати специалистов.
В настоящее время на «Мосфильме» также периодически организовываются курсы подготовки молодых пиротехников с моим участием. За время работы накопилось много материала, который может оказаться полезным современным пиротехникам.
Как развлечение пиротехника существует, наверное, с тех пор, когда дикий еще человек, наблюдая ночью за лесными пожарами, видел, что при падении горящих деревьев в небо поднимается масса красных и оранжевых искр. Он сидел на берегу широкой реки, понимая, что ему ничего не угрожает и любовался зрелищем.
С тех пор прошло много времени, но и поныне человек зачарованно смотрит на огонь, будь то пламя костра или топка камина. Когда же нам показывают фейерверк — тем более хочется смотреть, не отрываясь, чтоб не пропустить что-то интересное. А в фейерверке интересно все!.. Так это сегодня. Но для этого надо было пройти большой и долгий путь.
Колыбелью пиротехники, необходимо признать Азию. Китайцам за несколько столетий до нового тысячелетия были известны смеси, подобные пороху, которыми они пользовались для военных целей и изготовления различных цветных огней и ракет. Индусы, первые изобретатели бенгальского огня,

также устраивали фейерверки в давние времена, главным образом, в дни религиозных праздников. У них, как и у китайцев, имеются первые указания относительно применения горючих и взрывчатых смесей.
Прошли многие годы с тех пор, как европейцы проникли в Китай и Индию, узнали рецепты пиротехнических изделий и привезли их в Европу. Несомненно, что развитию пиротехники способствовали алхимики, от них пиротехника заимствовала эмпирические, иногда случайные смеси, найденные при производстве алхимических опытов.
Еще лет двести назад под словом «пиротехника» понималась вся совокупность знаний и приемов, необходимых для изготовления пороха, взрывчатых смесей и самых разнообразных пиротехнических составов. Однако еще раньше, в XIV веке, с изобретением дымного пороха, благодаря которому появилась возможность регулировать быстроту горения путем изменения количества компонентов в дозировке различных изделий, наступил коренной поворот в пиротехнике. В военном деле значительно расширились возможности успешных действий против неприятеля с применением пороха. В увеселительном, фейерверочном направлении мастера, изучая и пробуя, находили новые рецепты смесей, придумывали еще невиданные изделия и демонстрировали свое искусство. В это же время пиротехника разделилась на военную и гражданскую, постоянно обогащая и дополняя одна другую, делясь новинками, найденными в процессе работы и опытов.
О том, что на Руси в большом количестве и отличного качества производился черный порох уже в XV веке, мы можем судить по документам, историческим ссылкам, дошедшим до наших дней. Это был первый настоящий пиротехнический состав. При Иване Грозном в XVI веке и артиллеристы — пушкари и пороходельцы, непосредственно изготавливающие пороховые смеси, были преимущественно из коренных русских. Уже в то время пороха в России производилось до двадцати тысяч пудов. Русское войско умело использовало силу и эффект пороха, что известно из истории взятия Казани после длительной осады. В начале XVII века русский пушечный мастер Онисим Михайлов написал дошедший до наших дней «Устав ратных, пушечных и других дел, касающихся военной науки». В этом труде, представляющем практическое руководство для русских артиллеристов, изложены и сведения о ракетах.
Есть свидетельства, что в 1674 году в городе Устюге был устроен фейерверк. Было пущено несколько тысяч ракет и’шутих. Русские пиротехники нисколько не уступали европейским коллегам в деле изобретательности, исканий и находок в опасном, но интересном огненном искусстве.
Известно, что такие гениальные люди русской истории, как Петр Великий и всемирно известный ученый, основатель московского университета М.В. Ломоносов, не только поощряли фейерверки, но и принимали личное участие в их изготовлении и пусках.
При Петре I фейерверки становятся неотъемлемой частью увеселений, устраиваемых по случаю

____ ПИРОТЕХНИК
J «JAWWOMBlW ■ ■>>" *>*НЙ«»Й>Ж*йи«*<ШИ*ММММММЦ^*>^ НІЧНІ ММ 1 у» IT II Trt.4 і і >і ІШ rtfrrr [TTfflttfrtTj 'ІЇІ.П w .1 и * MJU дж,г ІІЖЙГГП urn -каких-либо торжественных событий. В то время фейерверки были весьма дорогими, но император не жалел денег на их устройство. Он собственноручно изготовлял ракеты, шутихи, огненные колеса и картины; им же было основано специальное «Ракетное Заведение». Имеются личные записи Петра I о составах фейерверков. Он планировал картины и ход всего фейерверка по нарастающей. Основная его идея заключалась в том, чтобы самым мощным и зрелищным был финал.
По приказу Петра Великого осветительные ракеты применяли в армии как средство сигнализации. При нем в Петербурге был основан Охтенский пороховой завод и значительно увеличено производство пороха. Заводы эти существуют до нашего времени. Гениальный русский ученый М.В. Ломоносов за годы пребывания в Академии наук осуществил много выдающихся фейерверков. Сохранилась гравюра, изображающая фейерверк, изготовленный «по изобретению Г. Советника и профессора Ломоносова» оберфейерверкером Матвеем Мартыновым и сожженный в Москве на новый 1754 год.
В одном из отчетов о работах за 1756 год М.В. Ломоносов пишет: «Пункт 3. Ныне лаборатор Клементьев под моим смотрением изыскивает по моему указанию, как бы сделать для фейерверков верховые зеленые звездки». Не считал «мелочью» такой великий человек сделать на радость людям «верховые зеленые звездки», которые тогда еще не были известны. Теперь каждый пиротехник знает, как сделать несколько различных смесей, из которых потом можно изготовить «верховые зеленые звездки».
Русские фейерверки достигают во второй половине XVIII века наибольшего блеска и изящества.
Исторический очерк
Фасады фейерверочных фронтов делались тогда огромных размеров: до 100 метров по фронту и до 50 метров в высоту. Зрелища собирали большое количество народа, они продолжались от десяти минут до получаса, повторы фигур и картин, изделий и эффектов если и допускались, то не поощрялись. В те времена пиротехника еще не базировалась на химии и физике. Считалось, что достаточно быть большим практиком. Конечно, мастера-пиротехники отличались огромными знаниями, основанными на большом личном опыте, на опыте предшественников-учителей. Даже в печатных трудах, очень редких в то время, как, например, «Катехизис пиротехника», написанный и опубликованный пиротехником Нида, не ставили вопроса о знании химии, исходя из того, что одна практика создала гениальнейших пиротехников, известных во всем мире. Однако так считали не все пиротехники. В конце XVIII века появился в Москве печатный труд русского оберфейерверкмейстера М.В. Данилова с длинным названием «Довольное и ясное показание, по которому всякий сам собой может приготовить и сделать великие фейерверки и разные иллюминации». Книга эта была лучшим руководством и справочником по пиротехнике в течении десятков лет. В это время изготовление и пуски фейерверков самодеятельными пиротехниками и в государственных заведениях достигают такого количества и размеров, что правительство России сочло необходимым регламентировать их специальным «Положением о фейерверках». Это был первый закон об упорядочении изготовления и пусков фейерверков. К тому времени уже пострадало много людей и случилось много пожаров.
ПИРОТЕХНИК

В начале XIX века издана книга Ф.С. Челеева «Полное и подробное наставление о составлении увеселительных огней с присовокуплением приготовления военных огнестрельных и зажигательных вещей». Эта книга обобщала все достижения в пиротехническом искусстве: как в военном, так и гражданском. Она состояла из пяти частей, и последняя, пятая, часть давала описание изготовления различных зажигательных и светящихся ядер.
В1832 году при Охтенских пороховых заводах была создана Пиротехническая школа с пятилетним (!) учебным курсом. Ее ученики обучались изготовлению пороха, военно-лабораторному делу и приготовлению фейерверков. Государство признало, таким образом, полезность и необходимость иметь грамотных во всех отношениях пиротехников и руководителей пиротехнических заведений и мастерских. В эти же годы в России стали изготовлять составы цветных огней с бертолетовой солью, и фейерверочные средства обогатились нововведениями: применением в фейерверках боевых ракет и ракет с парашютом. К этому времени организуются специальные ракетные заведения. Важную роль в пропаганде пиротехники в России играл «Артиллерийский журнал», публиковавший все передовое, что появлялось не только в России, а также переводные статьи из европейских публикаций, касающихся данной темы. Так, в 1839 году в нем Свечников опубликовал большую статью «О фейерверочных составах», в которой подробно и со знанием дела разбираются свойства различных составов цветных огней. В 1841 году журнал публикует несколько статей пиротехника Фадеева о составах красного и синего огней.
-10-

Исторический очерк
—і ■ wawmtrrr' и.шж wn^Wwawwamiii мгтгггішмуімггіот
В сороковых годах XIX столетия начал свою деятельность выдающийся русский пиротехник К.И. Константинов, Свои статьи он печатал также в «Артиллерийском журнале». В конце сороковых годов он приступил к систематическому конструированию и производству боевых ракет. С 1850 по 1859 год К.И. Константинов возглавляет Петербургское «ракетное заведение», где осуществляет ряд серьезных научных экспериментов, создает несколько новых систем ракет, которые успешно применялись в турецкой войне 1853 1855 годов. За свою недолгую жизнь этот талантливый человек написал и опубликовал более пятидесяти работ, в том числе большую статью «Усовершенствование фейерверков». Трудно переоценить тот огромный вклад, который сделал К.И. Константинов в развитие пиротехники — и военной и фейерверочной.
Еще при жизни Константинова в Москве в 1852 году была издана книга П. Румянцева «Теоретическая и практическая пиротехника», в которой обобщались многие находки и изыскания в данной области искусства.
Небольшая, но хорошо написанная книга известного впоследствии русского ученого с мировым именем в области электротехники В.Н. Чиколева под названием «Руководство к приготовлению и сжиганию фейерверков с описанием Электрического освещения» вышла в Москве в 1868 году и выдержала пять (!) изданий.
Специальные пиротехнические исследования производились в Михайловской Артиллерийской Академии, образованной из офицерских классов
-11-
артиллерийского училища в 1855 году. В этой Академии читал лекции К.И. Константинов. В это время, во второй половине XIX века, в пиротехнические составы начали вводить многие новые материалы, обогащавшие зрелищность фейерверков, их эффективность.
В 1861 году появилась небольшая, но весьма серьезная и полезная по содержанию брошюра Ф.Ф. Ма-тюкевича «Собрание формул и рецептов составов потешной пиротехники».
В 1869 году А.И. Плесцов опубликовал в «Артиллерийском журнале» статью «Об употреблении магния в пиротехнике. За два года, с 1887 по 1889, в «Артиллерийском журнале» помещаются новые статьи по пиротехнике: капитана А. Ордынского — «Пиротехнические заметки», Ф.Ф. Матюкевича — «Исследование составов белого огня с магнием и другими телами», П.С. Цытовича — «Пиротехнические составы» и «О пиротехнических формулах».
В девяностые годы XIX века выходит большое количество руководств по развлекательной пиротехнике, т.е. по изготовлению и сжиганию фейерверков, лучшими из которых, несомненно, надо считать появившиеся почти одновременно в 1894 году обширные, фундаментальные труды под руководством П.С. Цытовича и В.Ф. Степанова. Три года спустя, в 1897 году в литографированном издании Михайловской Артиллерийской Академии выходят лекции профессора А.В. Сапожникова под общим названием «Военная пиротехника».
В начале XX века в связи с разработкой электролитического способа получения алюминия, в
пиротехнике начали применять термитные составы, реакции горения которых открыл и изучал еще в 1865 г. академик Н.Н. Бекетов, русский физико-химик, основные исследования которого — в физической и неорганической химии. Н.Н. Бекетов, его ученики и последователи произвели многочисленные термохимические исследования. Он же впервые ввел в процесс обучения физическую химию как основную учебную дисциплину.
Есть косвенные доказательства, что и великий химик Д.И. Менделеев принимал участие в пиротехнических исследованиях. Его ближайший помощник, сотрудник Научно-технической лаборатории морского ведомства С.П. Вуколов работал над усовершенствованием сигнальных средств Морского Флота и над созданием первых образцов трассирующих снарядов. Смеси с применением магния и алюминия, железа и кремния постоянно были в поле внимания военных пиротехников.
С развитием военной техники до 1914 года, и особенно во время первой мировой войны, русская армия получила на свое вооружение значительное количество сигнальных, зажигательных, дымовых и осветительных средств. Над усовершенствованием осветительных средств — бомб, ракет, факелов в то время работал опытный и мудрый пиротехник В.А. Артемьев. Наряду с ним русские пиротехники Ершов, Горбов, Санников, Погребняков и другие практики и теоретики создали дымовые шашки, термитно-зажигательные снаряды, осветительные снаряды, сигнальные огни и многие другие пиротехнические боеприпасы.
-ZJ-

_____________ПИРОТЕХНИК
После первой мировой войны, которая привела к большому развитию всех военных разработок, гражданская пиротехника продолжала пользоваться пособиями старых мастеров: Степанова и Цытовича. Материалы о военной пиротехнике не могли публиковаться из-за шпиономании, хотя в закрытых и секретных лабораториях ученые ни на миг не прекращали работу. Только спустя многие годы, в 1927 году М. Петров опубликовал хорошее пособие «Общедоступная пиротехника». Затем в 1930 году Н. Александров выпустил полезную книгу для пиротехников-фейерверочников под названием «Пиротехника. Фейерверочное дело».
Хорошим пособием явилась книга «Химия горения» в 1935 году, выпущенная Б.Г. Тидеманом и Д.Б. Сциборским.
В конце тридцатых годов XX столетия, перед второй мировой войной, русские пиротехники выпустили целую обойму книг и пособий, и любой пиротехник, будь то профессионал или любитель, не смог бы доказать, какая из них лучше. Потому что все они были очень хороши.
1938 год. И.П. Толмачев. «Производство алюминиевого порошка, алюминиевой пудры и термита»; В.М. Солодовников — «Пиротехника (Производство и сжигание фейерверков)».
1939 год. Н.Ф. Жиров. «Свечение пиротехнического пламени» — труд, который просто невозможно переоценить; А.М. Демидов. «Введение в пиротехнику», В.Я. Смирнов. «Пиротехнические материалы».
1940 год. И.В. Быстров. «Краткий курс пиротехники», В.Я. Смирнов. «Введение в технологию
пиротехнических производств»; А.А. Фрейман. «Краткий курс пиротехники».
В течении этого десятилетия публиковались труды и по теоретическим вопросам, хотя такое определение можно дать с большой натяжкой, кроме уже упоминавшихся книг, появились в печати: 1937 год — «Курс теории взрывчатых веществ» А.А. Соколова; 1939 год — «Пиротехнические материалы» В.Я. Смирнова; 1936 год — «Теория взрывчатых веществ». К.К. Снитко; 1938 год — «Химия и физика маскирующих дымов» Ю.И. Вейцер и Г.П. Лучинский.
Наряду с оригинальными книгами, непосредственно описывавшими материалы изделия, монтаж и сжигание фейерверков, появлялись в периодической литературе различные статьи о новых материалах, внедряемых с большой пользой в пиротехнику, печатались переводы из иностранной периодики. Именно периодическая печать познакомила советских пиротехников с трудами В. Веллера, О. Векцельберга, В. Толглинсона, Конена, Зелена, Линце.
Я.Б. Зельдович смог опубликовать свою книгу «Горение и детонация в газах» в 1942 году. Стоит ли говорить о том, что в разгар Великой Отечественной войны такая область науки, как пиротехника, представляла собой большой интерес 'для иностранных разведок. Холодная война также не способствовала публикации новых открытий в данной профессии. И все равно в руководствах и рекомендациях оборонным заводам и производствам НИИ химии и физики в брошюрах с грифом «Совершенно секретно» или «Для служебного пользования» во множестве распространялась передовая пиротехническая мысль.
С большим трудом после довольно долгого молчания выходила на белый свет из глубокого подполья пиротехника. В технических журналах появлялись отдельные статьи, в которых пиротехники могли найти что-то новое для себя. В этом отношении полезным себя зарекомендовал журнал «Техника и вооружение», печатавший новости, которые пропускала цензура; наряду с ним публиковали интересные и познавательные общедоступные материалы журналы «Военный вестник», «Вестник связи», «Военно-исторический журнал», «Техника молодежи», «Новости техники» и др.
Именно из этих публикаций впервые мы узнали о синтетических и искусственных смолах, применяемых в пиротехнических смесях в различных сочетаниях, о применении циркония в особо ответственных изделиях. Потом стали доступны некоторые материалы по ракетной и космической технике. В 1951 году была опубликована книга Демидова «Основы горения вещества», давшая новое ускорение развитию пиротехнического искусства и многим новым работам в этой области. А.И. Лазарев и М.Ф. Сорокин в 1953 году обнародовали значительный труд «Синтетические смолы для лаков». При прессовании различных звездок появилась новая возможность выбора цементаторов. Все цементаторы в пиротехнических составах являются горючими, иногда дымообразующими или катализаторами, или замедлителями. Вместе со знаниями о смолах мы получили сведения и об их отвердителях, что значительно упрощало поиски новых рецептов и смесей.
Современную пиротехнику серьезные исследователи давно рассматривают как одну из самостоятельных отраслей знаний, требующую самостоятельной научной и учебной литературы. Ведь в пиротехнике существует целый ряд закономерностей, вывести и определить которые, оперируя только знаниями, взятыми из смежных научных областей, весьма трудно. Именно этим руководствовался замечательный пиротехник А.А. Шид-ловский, написавший и выпустивший свою книгу еще в 1943 году, которую назвал «Основы пиротехники». Эта работа была оценена не только гражданскими пиротехниками, но и стала настольной книгой для специалистов оборонной промышленности; высшие и специальные заведения использовали ее как учебное пособие при обучении студентов и слушателей. Практики-пиротехники получили научные практические советы и руководства из первых рук, ибо Шидловский А.А. посвятил всю свою жизнь разработкам, изучению и внедрению новых пиротехнических смесей и изделий, собственноручно проводя каждую задумку, каждый рецепт, используя и пробуя все новые и новые различные химикаты и материалы.
Десятилетие спустя, в 1954 году, он печатает в «Оборонгизе» несколько переработанный, с добавлениями и уточнениями, с привлечением наиболее знающих соавторов, труд под тем же названием «Основы пиротехники». Эту книгу Министерство высшего образования допускает в качестве учебного пособия для факультетов химико-технологических вузов СССР, для студентов других высших учебных заведений. Она содержит основные сведения о расчете и

________________________ПИРОТЕХНИК свойствах пиротехнических составов и весьма полезна для инженерного и технологического персонала заводов, цехов, мастерских, изготовляющих такие составы. Эта книга уже полвека является основным руководством при разработке новых и улучшении старых пиротехнических рецептов в пиротехническом цехе при киноконцерне «Мосфильм», где я имел честь отработать сорок три года. И в практической работе, при отыскании нового пиротехнического эффекта (кино!), и при обучении молодых специалистов-пиротехников замечательные книги Шидловско-го — главный и первый подсказчик и советчик.
При внимательном и вдумчивом чтении и изучении этих книг мыслящий пиротехник сможет сделать не только ночной фейерверк, но и дневное интересное, захватывающее зрелище из разноцветных дымовых, звуковых, свистящих и иных эффектов, спрос на которые растет год от года, день за днем.
Профессор Александр Александрович Шидлов-ский продолжал работать и время от времени печатал свои статьи в научных журналах. Двадцать лет прошло с выпуска его книги, найти ее было невозможно, и в 1973 году он выпускает вновь «Основы пиротехники» в издательстве «Машиностроение». В этом издании Шидловский расширил многие старые темы, появились новые описания: материалов и рецептов, дана характеристика многим новым изделиям. Стоит ли говорить, что ее тираж разошелся по стране в короткое время, а сегодня найти эту книгу крайне проблематично. Разве что наследники-старых пиротехников принесут букинистам книгу, ставшую им ненужной.
Так много рассказывая о трудах А.А. Шид-ловского, я нисколько не хотел умалить значение других авторов, каждый из которых в свое время внес большой вклад в развитие пиротехнической науки и достоин огромной нашей благодарности.
Однако пиротехническая мысль не может стоять на месте. Будет полезно прочитать, а еще лучше иметь в своей библиотечке следующие издания:
Брауэр К.0. «Пиротехнические устройства для космических аппаратов». Вопросы ракетной техники, 1969 г., выпуск 10, стр. 47—61.
Васильев В.Н. «Старинные фейерверки в России», Издательство государственного Эрмитажа, 1960 г., 92 с.
♦ Вспомогательные системы ракетно-космической техники» (Сборник статей. Перевод с английского под ред. Тишунина И.В.). Москва, Мир, 1970 г., 400 с.
Инами И., Шенфилд X. ♦ Неакустические пульсации при горении перхлората аммония, содержащего алюминий». Ракетная техника и космонавтика, 1964 г., № 7, стр. 196 201.
Сарнер С. «Химия ракетных топлив» (Перевод с английского под ред. В.А. Ильинского). Москва, Мир, 1969г., 488 с.
Хартиг Г. «Спички» (Сокращ. перевод с немецкого). Москва, Лесная промышленность, 1975 г., 292 с.
В этом очерке я кратко рассказал о многих публикациях, но еще больше книг, очерков, статей осталось за рамками рассказа. Когда-нибудь появится историк пиротехнической науки — он расскажет более интересно и подробно обо всем материале, обо всех людях, пропагандировавших, разрабатывавших, искавших и находивших пути улучшения пиротехнических изделий, организации устройства и пуска фейерверков.
Необычайно широкий спрос на фейерверки в последние 10-15 лет породил и соответствующее количество предложений. Однако в такой специфической области деятельности, когда фейерверки и другие специальные эффекты в театрах, парках, при массовых гуляниях и праздниках, стали обязательными, участились и непредвиденные случаи с травмами, а иногда и трагическими последствиями. Появились и появляются новые полу-подпольные мастерские, где кустарными способами, с грубыми нарушениями требований техники безопасности изготавливаются пиротехнические изделия. Перед праздниками на городских рынках любому покупателю, даже детям открыто продают фейерверочные изделия сомнительного производства и неизвестного срока их изготовления. На просроченную продукцию иностранного производства наклеивают российские этикетки и инструкции, а изделия уже давно непригодны и даже опасны для использования.
И магазины, торгующие пиротехнической продукцией, и склады сосредоточены в крупных городах, а праздники проходят даже в мелких населенных пунктах, и там тоже хотят видеть фейерверки. Однако изготавливать фейерверочные изделия подпольно, на кухне или на даче в сарае было бы архиглупо. Большинство химикатов ядовиты, пылят, а значит, как ни оберегайся — часть из них может попасть в пищу домашним или гостям. В сарае пыль будет скапливаться в разных местах, и смешиваться будут самые опасные несовместимые химикаты. Результат? Рано или поздно — пожар! Есть один реальный путь — законно, по всем правилам, открыть легальную пиротехническую фейерверочную мастерскую с разрешения и под эгидой всех местных властей от санитарно-эпидемиологического надзора, пожарных, милиции до главы управы, муниципальной администрации, и главы района. Все они лично заинтересованы в нормальных, веселых праздниках в вашем городе. Хороший фейерверк собирает людей больше, чем заезжие гастролеры-эстрадники, хотя они и дополняют друг друга.
Всякий пиротехнический эффект происходит в результате процесса горения, представляющего собой окислительно-восстановительную реакцию, при которой окисление одних компонентов протекает одновременно с восстановлением других.
При горении веществ повышается их температура, и это ведет к образованию пламени, свечению или выделению дыма. Для получения того или другого эффекта пиротехнические составы сжигают на открытом воздухе либо в смесь с горючими веществами вводят вещества, богатые кислородом и способные легко отдавать его. Такие вещества называются окислителями.
Почти все пиротехнические составы содержат окислители, в качестве которых применяются соли хлорноватой, азотной и других кислот, перекись бария, окислы. железа, марганца и свинца.
В качестве горючих материалов используются металлы: Mg, Al, Си, Be, Zn, Fe, Sb; неметаллы: P, S, C, Si, В; органические и неорганические соединения: бензол, толуол, нафталин, антрацен, парафин, сульфиды, карбиды и другие.
Смесь из горючего вещества и окислителя называется основной двойной смесью. На основе двойной смеси приготавливают различные пиротехнические составы. В зависимости от требований, предъявляемых к составу, в основную смесь добавляют различные добавки — компоненты.
Понятия и термины пиротехники
Для придания составу механической прочности используются вещества, способные связывать состав при его прессовании. Такие вещества называются цементаторами. Обычно они бывают и горючими. В качестве цементаторов применяются идитол, бакелиты, канифоль, шеллак, олифа, клей (декстрин), различные лаки и другие.
Для уменьшения активности пиротехнических составов и понижения их чувствительности к механическим и тепловым импульсам в составы добавляют вещества, замедляющие процесс горения — флегматизаторы. В их число входят парафин, канифоль и некоторые масла.
Для ускорения процесса горения в составы вводят вещества, называемые активаторами. К ним, например, относятся перекись марганца, тиомочевина и другие химикаты.
Вводя в состав различные компоненты либо меняя их количественное соотношение, можно регулировать течение процесса горения в соответствии с требованиями, которые предъявляются к пиротехническим изделиям различного назначения.
Для получения пламени определенного цвета, регулирования температуры горения и некоторых других целей используют цветнопламенные добавки — вещества, участвующие в реакции горения и окрашивающие пламя или дым.
Каждое вещество при горении излучает свой особый, характерный спектр. Если вещество в раскаленном состоянии излучает световые лучи определенной длины волны, то такое лучеиспускание называется избирательным.
ПИРОТЕХНИК И<ЖІШМІЙІГ.Т.Г'Л''ІЇІТҐІ',Г<.ГІҐ ~ГҐ У'.т."'"'ЛJ'fTir.f'Jrm’LnUHmriWMiHii~||ЦТГЦМи.г.iiLM/J*ri>rjxn>wti(M|><*lWlMlM>lMlllj№1IlJ.riTlX*iJ.r»M|llW\
Для получения пламени, окрашенного в определенный цвет, используются только те вещества, свечения атомов которых при реакции горения дает яркие полосы в определенной видимой части спектра. В пиротехнике используют атомарное свечение натрия и молекулярное свечение стронция, бария, меди и других веществ.
В сигнальных и осветительных составах боевого и народнохозяйственного назначения применяются огни красного, желтого, синего, зеленого и белого цвета. Для подачи различных сигналов, для создания самых разнообразных эффектов используются цветные и белый дымы, широкая гамма цветных дымов с довольно точным и определенным химическим составом рецептов. Постоянно совершенствуются и пламенные составы, а также изделия из них.
На больших расстояниях лучше всего различим красный цвет. Объясняется это тем, что лучи красного цвета из всех видимых имеют наибольшую длину волны, равную приблизительно 0,75 мк, и атмосфера пропускает их лучше других лучей; кроме того, они меньше других рассеиваются в воздухе. Цветность красного огня с увеличением расстояния изменяется незначительно.
Пламя красного цвета получается за счет молекулярного свечения стронция, соединения которого входят в пиротехнические составы. В качестве солей, окрашивающих пламя в красный цвет, обычно применяют карбонат, оксалат, нитрат и иногда сульфат стронция. В нашем цехе наибольший расход солей стронция приходится на нитрат (Sr(NO3)2), хотя расходуем и другие соли стронция, правда, в меньших количествах.
Понятия и термины пиротехники
WJJWW,1,1,7, t ЩИ*,1 <> і > If»Ч‘|‘,‘ WJWWlW*WWWW*WB*—**ЙИЙ^ЯЙ^МИ»^ГИГММ.ІГВ>МИI
Для получения желтого пламени используется атомарное свечение натрия. Наилучшую окраску пламени в желтый цвет дает оксалат натрия (NaC2O2). Для увеличения силы света огня и яркости окраски пламени в пиротехнический состав иногда вводят магний (Mg), который подразделяется по номерам в зависимости от размеров металлических зерен.
Пламя синего цвета (голубого) получается на основе излучения монохлорида меди (CuCl), который образуется в результате разложения соединений меди под действием мощного теплового эффекта, то есть высокой температуры, при которой происходит реакция. Коротковолновые лучи синего пламени существенно рассеиваются в атмосфере и с увеличением расстояния приближаются по цвету к желтому. Поэтому пламенные пиротехнические составы синего огня не получили пока большого распространения как в оборонной промышленности, так и в фейерверочном искусстве.
Пламя в зеленой части спектра дает моно-хлорид бария (ВаС1). В некоторых случаях используют свечение атомов таллия (Т1). Этот последний элемент в нашем производстве не употреблялся из-за большой цены на него. Однако в мировой литературе по пиротехнике упоминаются некоторые пиротехнические изделия с применением таллия.
Если возникает необходимость получить оранжевое или фиолетовое пламя — смешивают различные цветнопламенные добавки и вводят их в пиротехнические составы. Например, если включить в состав красного огня соли натрия или в состав желтого огня соли стронция, то можно получить пламя оранжевого цвета. Если смешать в определенных


ПИРОТЕХНИК I адммижи*і>*тогггґ.ї । млин .vz. ї- ||
пропорциях составы синего и красного огней, то J образуется фиолетовое пламя, как на палитре жи- 1 вописцев.
В пиротехнические составы некоторых фейерве- ! рочных форсовых изделий часто добавляют различные металлические опилки. При горении пиротехни- 1 ческих составов опилки раскаляются, выбрасываются 1 .наружу и, сгорая в воздухе, дают эффект искрения. Цвет искр зависит от свойств металлов: стальные | опилки дают белые искры, цинковые — голубые искры, зерна древесного угля дают красные искры и j т.д. Надо отметить, что такие искры малоэффектив- I ны по сравнению с искрами, которые предложил и 1 внедрил В.Ф. Пугачев. Особенность его искр состоит в том, что они, вылетая в воздух, горят ярким бриллиантовым цветом, что дает эффект, не сравни-мый ни с какими опилками, но эти искры еще в воздухе делятся на несколько частей, напоминая микровзрывчики с разлетом мелких искринок в разные стороны. Когда «работает» форс, начиненный і составом с этими ибкрами, его не спутаешь ни с одним другим изделием. Рецептура и технология изготовления этого подсобного изделия будут даны ниже.
Искрение бывает двух видов: форсовым и шлаковым. Форсовое искрение вызывается неполным сгоранием частиц вещества, которые выносятся газами за пределы пламени и изделия и догорают в воздухе, как было сказано о бриллиантовых искрах. Шлаковое искрение происходит за счет разбрасывания раскаленных частиц продуктов горения состава. Именно в форсбвых изделиях употребляется крупка бриллиантового огня. Попутно заметим, что
Понятия и термины пиротехники 11'1 Гі*МИ ■»»11 МИ И 11 |i U 11^ I l'i ^|ii 1 Fj^f
идет поиск рецептуры и других цветов на основе пиротехнических составов для форсовых изделий для замены металлических опилок. Цветные искры, получаемые за счет опилок различных металлов, малоэффективны.
Надо заметить, что большинство видов горения пламенных составов хорошо видно ночью и в переходное время — сумерки. В дневное время лучше видны эффекты, исполняемые пиротехниками: взрывы, огненные фугасы, пожары, дымы различных цветов.
Дымы относятся к категории аэрозолей. Дымом называется скопление в воздухе тончайшей взвеси частиц твердых веществ. Размеры частиц дымовой системы чрезвычайно малы, их размеры бывают от 1 до 100 микрон. Цветные дымы получают двумя способами: дисперсионным, то есть путем распыления вещества в воздухе, и конденсационным, то есть путем химической реакции или возгонкой органических красителей. У нас в цехе павильонный дымсостав, смеси для шашек МПШ-5, МПШ-6, МГПІТ З, шашек черного дыма № 1 и № 2 и многие смеси других изделий разработаны на основе химической реакции, а основная масса цветных дымов — на основе возгонки органических красителей. Во втором случае пиротехнические смеси выделяют дым, существо которого состоит в том, что окрашенные вещества при их нагревании переходят непосредственно из твердого в газообразное состояние. Возгонка осуществляется в дымовой шашке за счет тепла (t°), выделяющегося при горении основной пиротехнической смеси. Температура горения дымовых составов 800-1200°С.
Для образования цветных дымов используют органические красители и полупродукты. Красный дым в основном дает родамин; желтый — ларанит-роанилин, аурамин; синий получают из индиго и ультрамарина, а черный — при горении металлохло-ридных смесей с некоторыми углеводородами (нафталин, антрацен).
Надо знать и то, что на глаз лучше других наблюдаются клубы оранжево-красного дыма (длина волны спектра 0,57—0,75 мк) и желтого дыма (длина волны 0,55-0,58 мк), так как глаз человека наиболее чувствителен к лучам именно этой части спектра. Это явление объясняется тем, что глаз больше всего приспособлен к солнечному свету, содержащему в основном желтые лучи, а также оранжевые и немного красных.
Для воспламенения любого пиротехнического состава необходимо затратить определенное количество энергии. Эта энергия называется начальным импульсом. В качестве начального импульса могут быть использованы механическая, химическая, тепловая, лучистая и другие виды энергии, оказывающие тепловое воздействие.
Характер горения пиротехнического состава во многих случаях зависит от вида начального импульса. Например: один и тот же состав при воспламенении его от искры горит сравнительно ровно и медленно, а при воздействии на него более мощным импульсом — взрывается (шашки черного дыма некоторые пиротехники использовали как ВВ при мощном детонаторе).
Каждый пиротехнический состав воспламеняется при определенной температуре. Температура, при которой начинается горение пиротехнического состава под воздействием пламени, называется температурой воспламенения. По температуре воспламенения того или другого пиротехнического состава устанавливают безопасный режим производства, хранения и применения пиротехнических изделий, изготовленных из этого состава химикатов.
Часто пиротехнический состав, подвергающийся нагреву, воспламеняется самопроизвольно, без воздействия на него открытого огня. Температура, при которой в условиях нагрева состав самовозгорается, называется температурой возгорания. Для многих пиротехнических составов она равна 250°С.
Можно значительно снизить температуру самовоспламенения, вводя в пиротехнический состав хлораты. О хлоратах, об их применении в нашем производстве речь будет идти ниже.
Пиротехнические составы, при горении которых образуется интенсивно светящееся пламя, называются пламенными составами. Сила света пламени, как и его окраска, зависит от свойств компонентов (химикатов) состава и конечных продуктов горения (реакции). Одна из задач, которую ставил перед собой автор данной книги, состоит в том, чтобы максимально раскрыть свойства химикатов — компонентов, наиболее часто встречающихся в рецептах изделий нашего производства. Температура горения большинства пиротехнических пламенных составов колеблется от 2000 до 3500°С.
К основным физико-техническим свойствам пиротехнического состава относятся: чувствительность, стойкость, гигроскопичность, взрывчатые свойства и скорость горения состава.
Чувствительностью называется способность пиротехнического состава реагировать на воздействие начального импульса, то есть пламени, удара, трения и т.д. Она зависит от химических свойств веществ, входящих в состав, степени их измельчения, примесей, содержащихся в компонентах, и плотности состава. Чувствительность состава тем больше, чем выше степень измельчения состава и его компонентов, и тем меньше, чем более плотно спрессован состав. Посторонние примеси в основных компонентах уменьшают или увеличивают чувствительность пиротехнических составов. Поэтому, прежде чем вводить в состав тот или другой компонент, прежде чем пользоваться им, пиротехник обязан знать, на сколько процентов данный химикат состоит из чистого вещества. Большое значение в составах имеют фдег-натизаторы, снижающие чувствительность пиротехнических составов, и катализаторы — повышающие их чувствительность.
Характеристика чувствительности пиротехнических составов позволяет определить условия изготовления, режим хранения и методы применения всех без исключения пиротехнических средств и изделий.
Стойкостью называется способность пиротехнического состава сохранять свои первоначальные физические и химические свойства в процессе хранения, рассчитанные производством-изготовителем. Стойкость составов позволяет судить о качестве данного пиротехнического изделия. С течением времени состав претерпевает определенные химические и физические изменения, которые иногда настолько существенны, что изделие из такого состава становится непригодным, а порой даже опасным для хранения и применения. Причина этого явления в том, что отдельные компоненты состава самопроизвольно вступают в реакцию, в результате которой химическая природа их изменяется. Если при взаимодействии компонентов начнет выделяться тепло, то состав может самовоспламениться.
Значительное влияние на стойкость состава оказывают различные примеси, и в частности, вода (влага), которые способны вступать в реакцию с металлическими порошками, вызывая нагревание состава и, впоследствии, его самовоспламенение.
Физические изменения, возникающие в составе при его хранении, обусловливаются в основном увлажнением, которое приводит к частичному растворению компонентов, разрыхлению состава и деформации заряда пиротехнического изделия. Нередко изменения происходят в составе за счет явления возгонки летучих веществ смеси.
Гигроскопичностью называется способность пиротехнического состава или отдельного компонента поглощать влагу из окружающей среды, что способствует разложению и отдельных компонентов, и состава в целом. Гигроскопичность обусловливается, главным образом, физическим состоянием состава и зависит от плотности его в заряде и гладкости поверхности заряда. Разрыхленная смесь притягивает влагу в большей степени, нежели спрессованная. При прочих равных условиях гигроскопичность тем больше, чем выше степень измельчения компонентов пиротехнического состава.
Химические изменения состава, происходящие в результате его увлажнения, носят различный характер. Составы, содержащие в качестве горючего порошки металлов, а в качестве окислителей неорганические вещества, начинают разлагаться обычно из-за коррозии порошков металлов, которая подчиняется той же закономерности, что и коррозия монолитных металлов; однако порошки, имея большую удельную поверхность, корродируют намного интенсивнее.
Если состав не содержит металлических порошков, то при его увлажнении значительных химических процессов обычно не наблюдается. Увлажнение пиротехнического состава приводит также к понижению его специального эффекта: состав горит медленнее, не развивает при горении нормальной температуры, меньше излучает световой энергии. Надо заметить, что это явление, это свойство не всегда можно считать отрицательным. Знать же об этом обязан каждый пиротехник, и если пиротехнический состав увлажнился по каким-либо причинам, его обязательно надо проверить, а затем определить его пригодность для использования.
Наименее химически стойкими являются составы, содержащие магний. Поэтому каждый вид пиротехнических изделий имеет свой максимально допустимый срок хранения, по истечении которого использовать изделия без пробы недопустимо.
ПИРОТЕХНИК
. 1//]ШШШШ]ПЛЛШДіиіГНіЯтіЯІІІ Іі.ЦІїГі'ІІіаШ'ЦИГГаИ—Wff.Hfumtl ИГІІЇІ—МҐ IT і......f' " ~І Ґ ' Л 1і1ГТГіТ.7.7Г~.'.7.~
Однако приходится сталкиваться с фактами, когда указанный на упаковке срок хранения прошел, а фактически эти изделия еще могут храниться долгое время.
Для понижения способности составов поглощать из окружающей среды влагу, вещества компонентов покрывают защитной пленкой пластификаторов. К пластификаторам относятся парафин, олифа и некоторые другие масла, а также спиртовые растворы различных клеящих веществ. Спирт улетучивается, оставляя лаковое покрытие частиц химикатов (компонентов) в готовых пиротехнических составах.
Взрывчатые свойства состава выражаются в способности его давать при определенных условиях взрыв. Большинство составов, из которых изготавливают пиротехнические средства, рассчитано на равномерное горение — за исключением специально предназначенных изделий; такие пиротехнические составы обладают минимальными взрывчатыми свойствами или не имеют их совсем. Однако при определенных условиях, например, при сгорании состава в замкнутом пространстве или при воздействии на состав мощного, начального импульса, многие пиротехнические составы способны взрываться. Способны взрываться составы вспышек, если их использовать в намного увеличенных количествах, вопреки требованиям инструкций по их применению.
Взрывчатые свойства составов характеризуются скоростью детонации, бризантностью и фугасным действием. Скорость детонации — это скорость распространения реакции горения при воздействии мощного начального импульса. Для мно-
гих пиротехнических составов, которые способны детонировать, скорость детонации около 3000 м/сек, а для ВВ эта скорость 9000 м/сек. Составы, содержащие в качестве окислителя нитраты, имеют малую скорость детонации, не превышающую 1000 м/сек. Многие пиротехнические составы вообще не детонируют.
Бризантность, или мощность взрыва состава, оценивается количеством работы, которую этот взрыв может выполнить в единицу времени. Пиротехнические составы имеют малую бризантность.
Фугасное действие проявляется в способности состава расширять свой объем в начальный момент образования продуктов взрыва. Пиротехнические составы обладают сравнительно небольшой фугасностью.
Под скоростью горения пиротехнического состава понимается время в секундах, в течение которого горение распространяется на 1 см длины заряда. Скорость горения пиротехнического состава зависит от свойств окислителя и горючего, степени измельчения веществ и плотности смеси. Например, хлораты в смеси с горючими веществами горят значительно быстрее, чем нитраты с теми же горючими. Чем больше измельчены вещества, тем выше скорость горения смеси; спрессованные составы горят медленнее. Кроме того, с повышением внешнего давления и начальной температуры состава скорость горения возрастает, в разреженной среде горение смеси происходит медленнее. Если горение происходит в замкнутом объеме, то давление образующихся газов и скорость горения возрастают настолько, что происходит взрыв.
Большинство заводских пиротехнических изделий приводится в действие с помощью капсюля-воспламенителя путем накалывания, удара или резкого трения специальных материалов, к которым относится порох, пороховая мякоть, подмазка, стопин, огнепроводный (бикфордов) шнур, спички различного назначения, факелы, электровоспламенители и другие.
Дымный или черный порох представляет собой механическую смесь серы, угля и калиевой селитры (нитрат калия). Смесь эта зерниста и обладает свойствами взрывчатого вещества. Температура вспышки пороха = 300°С, чувствительность к удару сравнительно невелика. Дымный порох используется в основном для изготовления различных вышибных зарядов, применяющихся в пиротехнике. К тому же среди взрывчатых веществ он значится как метательное взрывчатое вещество.
Пороховая мякоть — измельченный до тонкого порошка черный порох. Она более чувствительна к внешним воздействиям. Пороховая мякоть применяется в качестве воспламенительного состава во многих пиротехнических изделиях.
Подмазка — тестообразная смесь из легковоспламеняющегося вещества и какого-либо клеящего вещества: декстрина, крахмала, лаков. На производстве чаще других используется подмазка из пороховой мякоти. Подмазка наносится на те или иные части изделия и, высохнув, образует слой, который служит воспламенительным средством.
Стопин (нить стопина) — изделие из ниток или ткани, шнура, пропитанное и покрытое сверху горючим веществом. Основным стопинирующим веществом является порох или пороховая мякоть с добавкой клеящих веществ. Стопин предназначен для быстрой передачи огня от одной части пиротехнического устройства к другой.
Огнепроводный шнур служит для передачи огня заряду через строго определенное время после его поджигания. Шнур набит слабо спрессованным пороховым составом, через который пропущены хлопчатобумажные нитки, покрытые слоем асфальта или гутаперчи.
Спички состоят из двух элементов: терки и головки. Основой состава спичечной головки являются хлорат калия (бертолетова соль), сера и животный клей. Кроме того, в состав входит молотое стекло, железный сурик, цинковые белила (сухие) и другие вещества. В данной книге даются некоторые современные рецепты химикатов спичек-головок и к ним парные рецепты спичек-терок. В состав терочной намазки входят, как основные вещества, красный фосфор, антимоний, идитол, мел, двуокись марганца и некоторые другие материалы. Температура воспламенения головки обычной спички 220-315°С.
Терочные составы применяются также и непосредственно в самих пиротехнических изделиях и служат для воспламенения. Эти составы чрезвычайно чувствительны к трению и относятся к разряду материалов, весьма опасных при хранении и обращении.
ПИРОТЕХНИК
UJIHIiWJmH»WIHIWMIIWW,IIH/A»AWWtWWW8^mLUWJWn l,l,l,W,i,IIIIIIHr,IHIg№»l>IR>IHlWliril!»ril,l 1111МММ1МШМЙМ1МИ¥МИ1ГГГП*ГПТП>ПП1ППУ1^ЙВ№ЯЯИ»^
Капсюли, использующиеся в пиротехнических средствах, воспламеняются от накола либо от направленного удара. Капсюль представляет собой металлический колпачок, в котором сосредоточен заряд ударного воспламенительного состава. В ударный состав входят гремучая ртуть, антимоний, бертолетова соль и другие химикаты. Сверху состав закрыт кружком из оловянной или другой фольги. В нашем цехе изделия не снаряжаются капсюлями, но мы часто пользуемся заводскими изделиями, где воспламенителем является капсюль: патроны к стрелковому оружию, сигнальные патроны, шашки оранжевого дыма, плавающие и некоторые другие изделия и средства.
Факелы, как правило, изготавливаются пиротехниками из подручных материалов; основой их обычно бывает пакля и любое жидкое горючее от керосина, солярки до парафина. Хороши факелы из пористой резины — горят долго и пламя их имеет более высокую температуру.
Есть и другие средства воспламенения пиротехнических составов, но пользоваться надо теми, которые являются штатными для данного состава или изделия во избежание нежелательных последствий.
Мы выяснили, что для любого пиротехнического состава необходимы как минимум два компонента: окислитель и горючее. Так сложилось исторически, что первым в этой смеси называют окислитель.
Окислители
Технические требования к окислителям
Окислители: нитраты, хлораты и другие химикаты — поставщики кислорода для пиротехнических смесей, их роль в таких смесях; характеристика каждого окислителя с положительной и отрицательной их сторон; требования техники безопасности при работе с окислителями.
Ba(NO3)2 — нитрат бария, азотнокислый барий — получаются хорошие смеси с магнием (Mg) и алюминием (А1), а также цирконием (Zr), окрашивает пламя в зеленый цвет. Ядовит. Не гигроскопичен. В пиротехнике применяется технический продукт. При работе с азотнокислым барием необходимо следить за тем, чтоб были закрытыми органы дыхания, не допускать попадания пыли в глаза.
КС1О3 — хлорат калия, бертолетова соль — ядовита, токсична, взрывоопасна, может служить основой суррогатной взрывчатки при добавках нефтепродуктов, опасна с солями аммония (NH4) - не смешивать! Не допускать контакта! Опасна также с тиомочевиной (CSN2H4). В пиротехнических составах, применяемых в кинопиротехнике и, естественно, фейерверочном искусстве, КС1О3 является основой большинства изделий.
NH4C1O4 — перхлорат аммония, аммоний хлорнокислый — взрывоопасен, взрывается при температуре 1200°С. -Скорость детонации 2500—3500 метров в секунду. Хороший поставщик кислорода. Опасны смеси с бертолетовой солью из-за обменной реакции. Не допускать попадания перхлората аммония в смеси с бертолетовой солью.
КС1О4 — перхлорат калия, хлорнокислый калий — характеристики у перхлората калия примерно такие же, как и у бертолетовой соли, но его разложение ускоряется в присутствии железа (Fe), кобальта (Со), никеля (Ni), вольфрама (W) и всех-солей меди (Си). Хороший поставщик кислорода в пиротехнических смесях. Молекулярный вес = 139. Плотность = 2,5 г/см3; температура плавления = 570°С. Активного кислорода при сгорании участвует в реакции 46%. Применяется при изготовлении цветных огней. Собственное пламя окраски не дает, но усиливает цветность других компонентов, окрашивающих пламя.
KNO3 — нитрат калия, азотнокислый калий, селитра калиевая — основа пороха и многих пиротехнических фейерверочных изделий, по потребностям нашего цеха — второй химикат-окислитель. Молекулярная масса =101; плотность = 2,1 г/см3; температура плавления = 336°С, температура разложения = 700°С. Активного кислорода при сгорании участвует в реакции 40%. Благодаря относительно низкой температуре разложения применяется в воспламенительных составах. Легко отдает кислород, чем опасен в обращении. Токсических действий на организм человека не замечено.
Sr(NO3)2 — нитрат стронция, азотнокислый стронций. Бывает технический и «чистый». В пламенных пиротехнических составах окрашивает пламя в красный цвет. Применяется в пиротехнике «химически чистый», «реактивный чистый». Гигроскопичен. Молекулярный вес = 212; плотность = 2,9 г/см3. Температура плавления = 645°С, температура разложения ниже 600°С. Активного кислорода при реакции разложения участвует 40%.
NaNOg — нитрат натрия, азотнокислый натрий — химикат, который отдает 4 7% кислорода при реакции. Это один из высших показателей в дешевых окислителях. Другие показатели: молекулярный нес = 85, плотность = 2,2 г/см3; температура плав-нения = 308°С; температура разложения = 600°С. Очень хороший химикат. Однако из-за своей большой гигроскопичности не может применяться в двойных смесях с порошками металлов: Mg, Al, Zr (циркония) и других. Изделия с солями натрия (Na) требуют жесткой гидроизоляции и не могут храниться длительные сроки. Применяется в чистом виде, при горении дает чистое яркое желтое пламя. Работать с этим химикатом рекомендуется в респираторах и перчатках.
NaClO3 — хлорат натрия, хлорнокислый натрий — весьма гигроскопичен, в чистом виде редок. В условиях России ограничен. У нас на производстве не употребляется, за исключением лабораторных работ.
NH4NO3 — нитрат аммония, аммоний азотнокислый — в производстве употребляется «чистый» нитрат аммония. Сильно гигроскопичен, при относительной влажности атмосферы в 67% становится влажным, с порошками металлов составы весьма нестойки из-за агрессивности нитрата. Химикат мало чувствителен к трению, удару. Ядовит, защита органов дыхания и рук обязательны. В нашем производстве есть несколько рецептов изделий, куда NH4NO3 входит в качестве компонента.
Fe2O2 — оксид железа — плотный, тяжелый материал, применяется в зажигательных составах, в термитных изделиях; в нашем производстве редко употребляемый химикат. Не чувствителен к механическим воздействиям.
Fe3O4 — оксид железа, окись железа — кубические кристаллы темно-красного цвета. Не гигроскопичен, ядовит. При работе с оксидом железа необходимы меры защиты органов дыхания и открытых частей тела. В нашем производстве мало употребляется.
МпО2 — двуокись марганца, перолюзит — порошок черного цвета, применяется * химически чистый»; употребляется в зажигатель'ных смесях, отличный катализатор. В нашем производстве употребляется редко. Чувствительность к механическим воздействиям средняя.
ВаО2 — перекись бария — тонкодисперсный порошок белого цвета, применяется в воспламенительных составах, чувствителен к механическим воздействиям в смесях. При контакте с водой образует перекись водорода — Н2О2. Молекулярный вес перекиси бария = 169; плотность = 5,0 г/см3; температура разложения — 700°С; продукт не богат кислородом — при его горении кислорода участвует в реакции всего 9%. Химикат весьма токсичен. Ядовит. При работе с перекисью бария необходимы ме-ры защиты органов дыхания и открытых частей тела.
С2С16 — гексахлорэтан (ГХЭ) — применяется в дымовых составах; в смесях с порошками Mg, Al и другими активными металлами весьма чувствителен к механическим воздействиям — трению, удару. Ядовит. При работе с ГХЭ необходимо
ujHwmaruwiuijJiJi'irii wmWwwm *■ і мті*шіїпж'мтяммігвж^^ґґіітаи:тіі»цдід wmwwiwiimfiiw** »№> пользоваться противогазом, резиновыми перчатками. Проветривать помещение.
I С6С16 — гексахлорбензол (ГХБ) — применяется в дымовых смесях, менее ядовит, чем ГХЭ, можно работать в промышленных респираторах Ф-46 и РН-16; с порошками металлов также образует весьма чувствительные смеси; кроме того, пыль ГХБ опасна самовоспламенением от случайной искры. Не допускать пыли в рабочем помещении.
(C2F4)n — политетрафторэтилен, тефлон, флоулон, фторопласт — полимер, применяется в пиротехнических смесях в виде порошка, в дымовых составах. При нагревании тефлона выделяются токсичные продукты. Применение смесей с тефлоном в помещениях абсолютно запрещено. На открытом воздухе при пользовании пиротехническими средствами, содержащими тефлон, не допускать попадания дыма на людей, животных и птиц. Из-за токсичных свойств в нашем производстве тефлон малоприменим, однако пиротехники должны знать об этом окислителе.
Ф Промышленность вырабатывает много других окислителей, с развитием же химической промышленности их количество будет расти и, естественно, А мы не имеем возможности дать полную характе-■ ристику всем окислителям. Некоторые характери-* стики и свойства окислителей еще будут частично освещены при разборе компонентов рецептов пи-- ротехнических изделий. Однако надо соблюдать ос-■ новные технические требования к окислителям: і а) максимальное содержание основного веще-ft ства (обычно не менее 98—99%);
В б) минимальное содержание влаги (не более ■ 0,1-0,2%), при повышенной влажности окислители перед вводом их в пиротехнические смеси должны быть просушены;
в) минимальное содержание примесей гигроскопичных солей и солей тяжелых металлов (РЬ, Си и другие);
г) реакция водных растворов окислителей — солей должна быть нейтральной;
д) отсутствие горючих примесей и примесей твердых веществ (стекло, песок и другие), которые повышают чувствительность пиротехнических составов к механическим воздействиям (трение, удар);
е) отсутствие примесей, понижающих химическую стойкость или ухудшающих специальный требуемый эффект состава или пиротехнического изделия;
ж) перед вводом окислителя в пиротехнический состав строго соблюдать положение технологии изготовления данного изделия о степени измельчения химиката-окислителя, пропуская его через сито соответствующего размера ячеек.
Из различных таблиц, которые даются в виде приложения в конце книги, можно получить многие другие данные о свойствах не только окислителей, но и горючих, цементаторах, катализаторах и других компонентах пиротехнических составов.
Основные требования
Горючие-металлы, их порошки из частиц различного диаметра и их роль в пиротехнических составах; горючие-неметаллы; роль каждого из них в составах; характеристика каждого компонента-горючего; с какими химикатами нельзя смешивать и почему. Требования техники безопасности при работе с химикатами-горючими.
При выборе горючего надо учитывать многие факторы и свойства каждого из них. Для пламенных горючих это высококалорийные и средней калорийности порошки металлов, которые, окисляясь, дают необходимое свечение; для дымовых составов нужны горючие, образующие при своем сгорании большое количество газов; кроме того, еще и дымообразующие. Применяемые в пиротехнических составах горючие должны отвечать основным требованиям:
а) быть химически и физически стойкими при перепадах температуры от 60 до —60°С, быть по возможности устойчивыми к действию слабых растворов и щелочей, так как окислителями чаще всего бывают соли щелочных и кислотных металлов;
б) быть малогигроскопичными, еще лучше — не гигроскопичными;
в) иметь теплоту горения, обеспечивающую требуемый эффект наилучшим образом;
г) легко окисляться (вступать в реакцию) за счет кислорода окислителя или за счет кислорода среды;
д) требовать для своего сгорания минимального количества кислорода;
е) легко измельчаться (по возможности);
ж) не оказывать токсического действия на организм человека при обработке и не выделять токсических продуктов реакции при горении, потому что наши изделия употребляются, там где присутствует много людей.
Все горючие можно разделить на несколько категорий:
а) неорганические: металлы — магний, алюминий, сплавы алюминия с магнием в различных пропорциях и различного размера, реже сплавы циркония и сам цирконий, а также титан, цинк, железо, марганец, вольфрам, сурьма; неметаллы — фосфор, углерод (древесный уголь, сажа), сера; сульфиды фосфора (P4S3), сурьмы и другие, а также карбиды, силициды, фосфиды металлов.
б) органические горючие: бензол, толуол, нафталин, антрацен; углеводородные смеси — бензин, керосин, нефть, мазут, асфальты, сахар молочный и свекловичный, древесные опилки и сложные вещества других классов — стеарин, уротропин, дициандиомид, тиомочевина и другие горючие.
Основными горючими в пламенных пиротехнических составах нашего производства являются алюминий и магний, металлы более дешевые, чем цирконий, титан и другие редкоземельные элементы.
А1 — алюминий — металл, порошок, стружка. В пиротехнике применяется более пяти разновидностей порошка от пудры до № 1 (самого крупного) и стружки. Химически активен, дает хорошее свечение, окислению препятствует оксидная пленка — оксид (А12О3). Применяют в пиротехнике и сплав А1 с Mg (магнием) четырех фракций (размеров частиц) от крупного № 1 до самого мелкого № 4. С щелочными нитратами натрия, калия, лития быстро разлагается. Смеси с этими нитратами не рекомендуются. Лучший нитрат в смесях с порошками А1 — нитрат бария (Ba(NO3)2). Именно на этой смеси сделаны почти, все фотовспышки и другие пиротехнические изделия недлительного хранения. Нестойки смеси А1 с марганцево-кислым калием (КМпО3) из-за обменной реакции. Не рекомендуется смешивать порошки А1 (пудру тем более) с бертолетовой солью (КСЮ3), так как такая смесь весьма чувствительна к механическим воздействиям. Взвесь алюминиевой пудры в местах работы при большой концентрации в воздухе способна взрываться от малейшей искры.
Плотность А1 = 2,7 г/см3, температура воспламенения порошка № 4 на воздухе 800°С, температура плавления = 660°С, кипения 25ОО°С. Температура плавления оксида алюминия (А12О3) = 2030°С, температура кипения (с разложением) 3000°С. Количество А1 (в граммах), сгорающее за счет 1 грамма кислорода, — 1,12.
Mg — магний — металл, как и А1, магний в пиротехнике применяется в виде порошка. Он имеет четыре разновидности от номера 1 (МПФ-1) — магния порошок фрезерованный — до номера 4 (МПФ-4). В инертном газе в шаровых мельницах стружка после фрезерного станка дробится и просеивается на разных ситах. Отсюда получаются зерна Mg разного размера: №№ 1, 2, 3, 4. Магний очень активный металл, но его защищает, так же, как и А1, защитная пленка MgO. Оксидная плёнка Mg менее прочная,
ПИРОТЕХНИК
нежели Al, более пористая, и потому порошки магния в одинаковых с А1 условиях скорее приходят в негодность. Применяется магний в осветительных составах, составах цветных, фейерверочных, имитационных огней. Защита порошков магния в кислых смесях — различные масла, стеарин, парафин. Порошки магния не рекомендуется смешивать с хлоридом аммония (NH4C1), с серой (S) смесь магния недопустима. С тяжелыми металлами и их солями (Pb(NO3)2) — не имеет смысла из-за обменной реакции: (Pb(NOs)2 + Mg = Mg(NO3)2 + Pb. Смесь Mg + КСЮ3 не стойка из-за окисления, такой состав очень чувствителен к трению и удару. Плотность Mg = 1,7 г/см3; температура воспламенения порошка № 4 на воздухе = 550°С; температура плавления = 65О°С; температура кипения == 1100°С. Оксид магния MgO имеет температуру плавления = 2800°С. ПАМ — порошок алюмини-ево-магниевый — сплав А1 и Mg, также имеет размер зерен от номера 1 до 4. Надо отметить, что сплав алюминия с магнием в пропорции = Mg4Al3 содер жиг 54% магния, плотность его = 2,15 г/см3; температура плавления — 463°С. Этот сплав выгодно отличается от других сплавов Al+Mg тем, что меньше корродирует, весьма хрупок, и поэтому его легче измельчить. Соблюдать все предосторожности, как с порошками алюминия.
Zr — цирконий — в кинопиротехнике не применяется из-за дороговизны, применяется в пиротехнических замедлителях ракетной или космической техники. Весьма стоек к коррозии, к тому же порошок циркония почти всегда содержит значительное количество гидрида = ZrH. Грубые фракции порошков циркония воспламеняются при
температуре 180”200°С. Температура воспламенения тонкого порошка циркония 80-85°С. Работа с такими порошками опасна, особенно в условиях полукустарных производств.
Плотность Zr = 6,5 г/см3, температура воспламенения на воздухе = 180-200°С*, температура плавления = 1868°С; температура кипения = 475О°С. Водном грамме кислорода сгорает 2,85 грамма циркония. Оксид циркония ZrO2 плавится при температуре = 2700°С, кипит при температуре 43О0°С.
Ті — титан — в кинопиротехнике не применяется из-за высокой цены. Теоретические показатели титана очень хорошие. Смеси титана стойки к агрессивным химикатам. В оборонной промышленности используется в зажигательных и дымовых смесях, в ракетной и космической технике. Ті в последнее время стал доступен в порошках различной величины. Многие пиротехники используют его в качестве искрообразующего элемента. Фонтаны с порошками Ті пользуются большим спросом. Эффектны форсы и звездки из Ті.
S — сера — традиционное пиротехническое горючее. В пиротехнике применяется тонко измолотый порошок, очищенная от добавок сера применяется в дымных порохах, фейерверочных составах. При применении не путать с так называемым «серным цветом*. Это тоже сера тонкого помола, но добыта из конденсата и содержит большое количество серной кислоты. Составы с этим химикатом могут самовозгораться и поэтому опасны. Сера не токсична. Не рекомендуются двойные смеси с хлоратами из-за крайней опасности, может произойти самовозгорание на рабочем столе. Относительный атомный вес = 32,064; плотность — 2,06 г/см3; температура кипения — 444,6°С; в воде не растворима, в спирте плохо растворима; легко растворяется в сероуглероде: при 0°С в 100 граммах сероуглерода растворяется 46,1 г серы, при 55°С — 181 г. серы в 100 граммах CS2.
Форма кристаллов серы — ромбическая. Цвет желтый. Плохо проводит тепло и электричество. На воздухе сера воспламеняется при температуре начального импульса не ниже 260°С и горит слабым синим пламенем. Получают серу в виде минерала в земле, в горных породах, в горючих сланцах. Получают ее и из сероводорода, который содержится в природных газах. Твердость = 2,5. Удельная теплотворная способность 0,172 калории из грамма. Сера представляет собой важнейший носитель пламени в безопасной зажигательной смеси спичечной массы и является наилучшим горючим во многих пиротехнических рецептах.
Сера известна в этом качестве с незапамятных времен, то есть до изобретения пороха. В некоторых пиротехнических рецептах серу заменили канифолью или другими смолами, но благодаря тому, что при сгорании серы легче регулировать реакцию, сера, как и прежде, является основным носителем пламени в пламенных составах пиротехнических изделий. Активность обменной реакции серы зависит от удельной поверхности, от концентрации (количества в смеси) и от имеющегося кислорода. Исследования в отношении различных концентраций при постоянном содержании КС1Од показали, что содержание серы до 1% уже является достаточным, чтоб обеспечить горение, чтобы произошла реакция. При содержании в смеси серы более 1% быстро растет
Горючие
— ■ п-Д LTl I Ї1Г1ЇГПММГГП П.'Г.УЛ~1Т.ТГ11ГЙ ГJ/JW1' ''■'J'’-~-''.'l'_',f_T-~-r_'.'l.'.~.Tl'l<f Illi ШҐ 1"V " і Гі'1'W WlTT* fc—T «Г?"' 'Jf -? ■:: ■ ■ ^rrnrrnr
чувствительность состава к механическим воздействиям. Повышение содержания серы в пиротехнических составах более расчетных не способствует улучшению этих составов, смесей. Фактически при небольшом содержании серы (0,5—1%) и содержании хлората калия (КС1О3) около 50% в смесях обеспечивается хорошее взаимодействие, так как обычно в таких смесях присутствуют другие элементы и вещества, более того: в смесях излишнее содержание серы приводит к медленному горению этих смесей. Надо помнить, что большое содержание серы в рецептах и их изделиях увеличивает образование двуокиси серы — опасного химиката. Надо помнить и о том, что в порошке серы очень много примеси различных веществ, особо опасной является окись кремния (SiO2). Примеси в порошках серы других веществ приводят к значительному повышению чувствительности смесей с серой к механическим воздействиям. Поэтому степени чистоты серы следует придавать особое значение. Качество серы и ее чистота в рецептуре изделий нашего цеха в особых проверках не нуждается. Мы изготавливаем пиротехнические изделия с большим запасом надежности в отношении требований техники безопасности. Рецепты наших изделий рассчитаны на серу с большим допуском посторонних примесей. Но есть пиротехнические производства, где сера должна содержать в своей массе не более 1% посторонних примесей.
С — углерод. К углеродам относятся: алмаз, графит, древесный уголь, сажа. Алмазы — из-за дороговизны в пиротехнике не применяются; графит требует для своего воспламенения очень высокой
температуры и поэтому в пиротехнике почти не применяется. Нам остается сажа и древесный уголь. Условно именно древесный уголь мы называем «углеродом», именно о нем и будем говорить. Соединения с углеродом называются карбонатами. В таком углероде много других примесей — от 25 до 40%, (это зависит от температуры, при которой была сделана перегонка древесины в древесный уголь). Как горючее древесный уголь не стабилен, поэтому каждый раз, при поступлении новой партии древесного угля, прежде чем производить массовой серией какие-то пиротехнические изделия, древесный уголь надо проверить. Чаще всего приходится менять его соотношение как компонента по этим причинам. Для искрящихся составов удобен уголь, приготовленный из твердых пород лиственных деревьев: дуба, граба, бука, ясеня, березы, ольхи. Для подготовки пороховой мякоти, пороха, в форсовых составах лучше зарекомендовал себя уголь из мягких пород лиственных деревьев: липы, осины, тополя, ивы. Различить эти сорта угля можно по их твердости и звуку, который они издают при ударе. Твердые сорта дают «звонкий» звук. Уголь из хвойных пород деревьев в пиротехнике не применим. Большая концентрация угольной пыли, в помещении может привести к взрыву, поэтому помещения, где происходит размол, просеивание и развеска угля, должны часто проветриваться. При работе с углем надо пользоваться защитными средствами — респираторами, ватно-марлевыми повязками. Древесный уголь не токсичен.
Сажа — горючее, жирный уголь. Наравнё с древесным углем применима в пиротехнике; есть смеси с сажей цветных и белого дымов, искристые составы, где вводится сажа от 3% до 8%. Сажа — легковесный летучий материал, ее взвесь в воздухе помещения может быть большой концентрации. Это опасно в пожарном отношении. Сажа не токсична. Средства защиты органов дыхания, как при работе с углем.
В — бор, «аморфный бор» — порошок темно-коричневого цвета, имеет мелкий размол (дисперсность) менее 1 микрона, неметалл; рецепты с бором дают хорошие составы с отличными характеристиками, однако в гражданской пиротехнике применять бор (В) накладно из-за его дороговизны. Пиротехники кино с бором практически не работают, хотя возможности его велики.
Р (кр) — фосфор (красный) — порошок темнокрасного цвета, гигроскопичен, поэтому фосфор хранят в герметичной посуде. В соединении с влагой воздуха образуется фосфорная кислота (РН2О(0Н)2). В пиротехнике применяется с нейтрализаторами (окисью цинка, карбонатом кальция, окисью алюминия) и становится более устойчивым. Применяется и с клеевыми добавками: крахмала (С6Н10О5), декстрина (C6HWO5) на спирте.
Никогда нельзя делать сухих (без увлажнения) смесей фосфора с хлоратами — они образуют весьма чувствительные и потому опасные смеси. Нельзя смешивать сухие компоненты фосфора со всеми окислителями. Фосфор красный применяется в терочных, капсюльных, пистонных составах. Фосфор белый в пиротехнике не применяется. Работать с фосфором и его составами надо в респираторах и резиновых перчатках.
Si — кремний (силициум) — неметалл, хотя кремний обладает всеми характеристиками металлов, особенно в пиротехнике, где применяется как
ч&жщячсй&ыь ■ і гр itowwMimtHi rurii i ihwwj.wktamwmmwci* ш і ?
горючее; намного дешевле бора (В); темно-серый порошок. Сам не воспламеняется, но имея высокую температуру сгорания, Si применяется, в основном, в зажигательных смесях, в частности, в спичечной промышленности .
SbJSg — сурьма трехсернистая — антимоний. Цвет кристаллов оранжевый или черный, имеет характерный металлический блеск; измельчается легко; применяется во многих пиротехнических составах, в зажигательных, в бенгальских огнях, в терочных составах спичек, хлопушках. Сурьма трехсернистая чаще других сульфидов используется в пиротехнике и лучше других изучена и опробована на практике. Ее молекулярная масса + 340, плотность = 4,5 г/см3, температура плавления = 548°С. При сгорании получаются два продукта: Sb2O (окись сурьмы) и SO2 (сернокислый газ); за счет одного грамма кислорода сгорает 2,36 г сурьмы трехсернистой. Весьма активное горючее. При работе с антимонием работать необходимо в респираторе и резиновых перчатках.
Веретенное масло — в специальной литературе «промышленное масло» — нефтепродукт, плотность его = 0,88-0,89 г/см3; температура вспышки = 160°С. Используется в пиротехнике как предохранитель порошков металлов от окисления и разложения (Al, Mg и др.), составы с веретенным маслом хранятся значительно дольше, чем без него. Надо сказать и о том, что в пламенных составах масло несколько ухудшает эффект, выделяя при горении большое количество дыма.
Второе применение.веретенное масло нашло в нашем производстве при получении «тяжелого
-54-
Горючие .
Хыма* за счет возгонки при высокой температуре и мгновенном, резком охлаждении углекислым газом.
Скипидар — продукт перегонки смолистой древесины и смолы хвойных деревьев — растворитель лаков, смол, красок. Он отличается от предельных углеводородов (бензина, керосина, веретенного масла и прочего) большей легкостью окисления, легко воспламеняется при соприкосновении с концентрированной азотной кислотой. Смесь паров скипидара с воздухом взрывается. Работать со скипидаром рекомендуется вне помещений с большой осторожностью.
иементаторы
Их роль и значение в смесях
Соединения, химикаты, о которых пойдет речь ниже, выполняют роль в пиротехнических составах не только цементаторов. Чаще это — горючие, выполняющие роль и цементаторов, и горючих. Нам уже встречались сложные вещества, но то были окислители, которые еще и окрашивали пламя в определенный цвет, то есть несли двойную функцию в пиротехническом составе. Теперь пришла очередь познакомиться с горючими, которые выполняют и функции цементаторов. Надо еще оговорить и такие явления среди горючих, которые несут функции и катализаторов, газообразующих, дымообразующих, пламягасящих в дымовых составах, химикатах. За свою историю пиротехника, обогащаясь опытом и провалами, усилиями и исканиями многих поколений пиротехников, нашла много ценных и незаменимых компонентов в составах, которые выполняют не одну, а две, иногда три функции. И это не должно никого смущать, а, наоборот, служить к отысканию новых соединений, которые выполняли бы самые разнообразные функции в пиротехнических составах и стоимость их была бы наименьшей.
Углеводы
Крахмал — картофельная мука — для расчета в рецептах берется (C6HwO5)n —- пищевой продукт, в пиротехнике — вещество связующее горючее. Служит це-ментатором в цветных огнях, а также при изготовлении нити стопина. Является основой декстрина (С6Н10Ое).
Плотность крахмала = 1,6; в холодной воде почти не растворяется, в горячей растворяется значительно лучше. В кислой среде крахмал гидролизуется до виноградного сахара.
Сахар молочный — С12Н22ОПН2О — «лактоза»; получаемые из молока желтоватые, вязкие кристаллы. В смесях с хлоратами — весьма активное горючее, такие смеси чувствительны к механическим воздействиям. При невысокой температуре сгорания дает очень много газообразного продукта, хорошо окрашивающегося любым цветом красителя. Поэтому применим в цветных дымах. Плотность молочного сахара = 1,5 г/см3. Вода удаляется при температуре - 125°С; плавится при температуре около 200°С; с разложением на свои составные части. Молочный сахар безвреден.
Свекловичный сахар, тростниковый сахар — С12Н22ОП — пищевой продукт, как правило, в пиротехнике употребляется мало. Плотность его = 1,6 г/см3; плавится при температуре — 160°С; с небольшим разложением. Гигроскопичен. Пиротехнические рецепты ориентированы на молочный сахар — лактозу, который в пищу непригоден. Но при необходимости — эффект сгорания свекловичного сахара в пиротехнических составах тот же, что и при лактозе.
Древесина — (C6HwO5)n — мелкие древесные опилки — в древесных опилках очень много клетчатки, в сухих опилках примерно 2/3 от всей массы. В пиротехнических изделиях древесина оттеснена другими химикатами совершенно незаслуженно. Это дешевое горючее-связующее. В нашем цехе очень мало рецептов с древесными опилками. Древесина безвредна.
____ ПИРОТЕХНИК jrwnmwwri її ri и г п г г ■> итп і и иябіяя > । r гкіпімі—ийміиі і ff гм mmц»*шмхмйижвяиияю*в»іьки>6»і>и^^ чс
Стеарин — С17Н35СООН — точнеє, стеариновая кислота — продукт перегонки нефти; главное применение —. изолирующий материал частиц порошков металлов от коррозии, пропитки бумажных гильз для некоторых изделий; употребляется в спичечном производстве. Хорошее горючее-цементатор и гидроизолятор. По литературным сведениям применяется в качестве основного горючего при производстве пламенных пиротехнических составов различных оттенков голубого огня. Плавится при температуре = 71 °С, кипит при температуре = 359-383°С (при атмосферном давлении), плотность невелика = 0,94 г/см3. Давно подмечено пиротехниками, что стеарин активен поверхностно, поэтому в рыхлых составах его активность велика, а в спрессованных он позволяет гореть составу ровно — без скачков и затуханий. Стеарин — отличный пласти фикатор-горючее. Технический стеарин представляет собой смесь стеариновой и пальмитиновой кислот. При работе с расплавленным стеарином необходимы меры защиты органов дыхания.
Парафин — С26НМ — такая формула парафина условна, она используется для расчетов в рецептах, Парафин — смесь насыщенных углеводородов, продукт нефтеперегонки, белая или желтоватая масса без запаха и вкуса. Плавится при температуре = . 44 58°С, плотность = 0,88 0,91 г/см3. Парафин менее химически агрессивен, чем стеарин, и поэтому в составах с порошками металлов более предпочтителен, но менее, нежели стеарин, пластичен; однако, составы с парафином хорошо сохраняются в спрессованном виде. Защита органов дыхания при работе с парафином — ватно-марлевая повязка.
иементаторы
Upto.'.' ^^гіаооЙЯІЖЯРВДИВД^^ I.II^WU1*^ ^и'Д'И:*3»>«іа<а^У»^4УГ^г^*«rr <~|,'| w 1Г і MawnM*»TOKWffLTA7ff!,WjtTAra6 W wi
Антрацен — Cl4H10 — это белые кристаллы «чистого» антрацена, его плотность = 1,25 г/см3, температура плавления = 218°С, температура кипения = 342°С. Этот антрацен «химически чистый» и на его производство затрачивается много средств. Вводить его в составы черного дыма было бы большой бесхозяйственностью, и каждый килограмм состава или одна шашка черного дыма стоили бы так дорого, что затраты не оправдали бы доходов. Особенно на батальных кинокартинах. Изомер антрацена — фенантрен — имеет такую же формулу (С14Н10); по своим химическим и физическим свойствам — температура плавления = 99°С и температура кипения = 240°С еще более подходит для пиротехнических составов, так как для его реакции требуется меньше кислорода, а значит, и слабее окислитель или меньшее количество окислителя. Но фенантрен еще дороже антрацена. Мы же должны помнить всегда, что рецепт изделия должен быть из наиболее доступных и дешевых химикатов. Поэтому рецепты изготовления черных дымов разработали, основываясь на показателях технического антрацена, продукта весьма дешевого и не дефицитного в нашей стране.
Технический антрацен или то, что мы привыкли называть просто «антраценом», в массе своей содержит примерно лишь 25% чистого антрацена. 75% этой зеленовато-желтой или темно-зеленой массы составляют другие углеводороды. Если заняться разложением этого антрацена на отдельные фракции, его составляющие — мы можем выделить уже знакомый нам фенантрен (С14Н10), карбазол (C12H9N) и другие углеводороды, а также различные масла, в том числе и эфирные, летучие. Но именно наличие различных углеводородистых добавок и масел в тех ническом антрацене позволяет иметь вспышку антрацена уже при температуре = 150-165°С. С одной стороны, это не совсем хороший показатель для работы с техническим антраценом, так как низкая температура возгорания химиката — показатель его опасности при работе; с другой стороны, как уже было сказано выше, химикат с такой низкой температурой разложения будет хорошо реагировать е окислителем, имеющим небольшое количество кис лоро да или с небольшим количеством окислителя, богатого кислородом. Надо хорошо запомнить, что и антрацен (а речь идет о техническом антрацене, химикате весьма дешевом), и нафталин, и другие углеводородные соединения в пиротехнических составах выполняют роли не только горючих, но и дымо образователен, и газообразователей, что не менее важно, чем горючее в данных составах. Если бы нафталин и антрацен (а речь будет только о них, таї как мы видели, что другие углеводороды почти не приемлемы в нашем производстве по разным при чинам), были бы только горючими — мы бы от них отказались, потому что нам нужно дымообразова-ние, и чём большее дымообразовацие дает нам та или иная смесь или отдельный химикат, тем более приемлемы они. И одно дымообразование само по себе, без большого газообразования еще не есть ко нечный результат наших поисков. Когда же дымооб разование сочетается с большим количеством выделенных газов, которые окрашивают дым, — мы считаем, что рецепт нас устраивает. И все равно, какой бы хороший эффект мы не получили, при появлении новых химикатов пиротехники должны искать
и пробовать новые сочетания химикатов, новые рецепты, стремясь к наивысшему эффекту при самой низкой его себестоимости и наипростейшей и безопасной технологии его изготовления.
Вот один из примеров — рецепт черного дыма на металлохлоридной основе:
1. Гексахлоретан (С2С16) — 60%;
2. Магний порошок (Mg) — 19%;
3. Нафталин (С10Н8) — 21%.
Сейчас никто из пиротехников не делает такого состава черного дыма, хотя в свое время эта смесь была лучшей. Однако, когда нет других химикатов, а черный дым нужен, — поневоле сделаешь и такую смесь. Надо помнить, что смесь, сделанная по этому рецепту, не отвечает требованиям длительного хранения: сначала улетучивается ГХЭ, потом улетучивается нафталин, к тому же, что эта смесь чувствительна к удару. Здесь можно заменить летучий нафталин на такое же количество антрацена; смесь будет лучше по всем показателям, особенно потеряет чувствительность к удару, значит, станет безопасной в производстве, хранении, перевозках и при пользовании. А если гексахлорэтан заменить бертолетовой солью (КС1О3), химикатом, богатым кислородом, — можно отказаться и от металлического порошка-го-рючего — магния. И когда посмотрели смесь черного дыма: бертолетова соль, плюс антрацен — пришли к выводу, что эта смесь выгодно отличается по всем параметрам от смеси на металлохлоридной основе. Для того, чтобы это понять, потребовались многие годы, много было проб и ошибок. В нашем цехе было разработано много новых рецептов для изготовления черного дыма. Разработка новых рецептов — не самоцель, не игра в новое. Как правило, новые составы, образующие черный или белый дымы, как, впрочем, и многое другое, разрабатываются в крайних ситуациях. А такие ситуации складываются весьма часто. Поэтому знание химикатов, их свойств и характеристик придет на помощь в трудный момент коллеге-пиротехнику — такая у нас надежда, она-то и руководила нами при написании этого пособия.
Уротропин — C6H12N4 — гексаметилентетрамин — бесцветные кристаллы, хорошо растворяется в воде и потому весьма гигроскопичен. Получается при конденсации формальдегида с аммиаком. Содержит очень большое количество азота (N) и потому горит почти бесцветным пламенем, бездымен; применяется в цветных огнях; с небольшой добавкой окислителя имитирует горение газовых плиток. Многие пиротехники используют горение уротропина для создания эффекта «марево», когда воздух ко леблется от жары. Уротропин является главной составной частью при промышленном производстве так называемого «сухого спирта». Уротропина в воде (в 100 граммах) растворяется 167 граммов. В этиловом спирте малорастворим; термически стоек, загорается трудно, особенно на площадке противня, при создании эффекта «марево». При работе с уротропином необходима защита: респиратор, очки, резиновые перчатки. После работы необходимо принять душ. Уротропин ядовит.
Дициандиамид — ДЦДА (C24N4H4) — является в пиротехнических составах не только горючим, но еще и пламягасителем, поэтому в пламенных составах не применяется; широко применяется в цветных дымах. ДЦДА — кристаллы стекловидные; плохо растворяется в холодной воде, хорошо растворяется в ацетоне, в горячей воде, в подогретом спирте. При нагревании более 180°С разлагается, отщепляя аммиак, что можно почувствовать по запаху. При работе с дициандиамидом необходимы респиратор, резиновые перчатки, частое мытье рук.
Тиомочевина — CSN2H4(H2NCSH2) — кристаллический белый порошок — с хлоратами образует весьма активные составы, даже опасные, поэтому двойных смесей не рекомендуется делать. Тиомочевина содержит много азота, поэтому как горючее очень ценна, но имея в своей молекуле атом неокисленной серы, тиомочевина очень реакционна и тем опасна. Плавится при температуре = 182°С, плотность ее = 1,4 г/см3, в воде слабо растворима, поэтому считается не гигроскопичной. В нашем производстве тиомочевина применяется во многих пиротехнических изделиях, в цветных дымах, во вспышках, в имитаторах взрывов. Тиомочевина ядовита, при работе с ней необходимы меры защиты органов дыхания и открытых частей тела.
Связующие вещества
В своем производстве мы чаще других используем в роли связующих (цементаторов): масло веретенное, олифу натуральную, канифоль, декстрин; искусственные смолы: бакелиты, идитол, эпоксидные смолы, шеллак и другие лаки, но в пиротехнике применяют в качестве связующих нитроклетчатки, асфальты, битумы и растворы каучука. Требования к
igyswwwifiiiiMWW*wim^Mi^^iniwi>.«ftiiitwwwililWiWRiwiirMi waMTr^ij'a < i'j was** T»utry^i>i»MA^xxv<rri4iiLi^Lte^ifeb4jafw<>^ таким связующим веществам особые: они не должны растворяться в воде, иметь полную сопротивляемость гниению и разложению, что происходит с клеящими веществами животного происхождения; эти вещества должны растворяться в органических растворителях и иметь способность при высыхании к образованию пленки из своих растворов для надеж ной защиты от попадания влаги в готовое изделие.
Идитол — С13Н12О2 (условная формула для рас чета рецептов) — «но во лак», «новолачная» смола — комки янтарного цвета с красноватым оттенком. Получают конденсацией избытка фенола с формальдегидом в присутствии какого-либо кислого катализатора, например НС1. При обычной температуре легко измельчается в порошок. Можно вводить в пиротехнические составы в виде порошка с последую щим введением в состав спирта, можно и в виде спиртового раствора. При высыхании спирт улетучивается, идитол же остается прочной пленкой. Меры защиты: респиратор, перчатки, проветривание помещения, где работают с идитолом. Идитол хорошо растворя ется в этиловом спирте, у нас в цехе он — горючее-связующее во многих рецептах цветных огней; отличный цементатор. Температура его размягчения 97~100°С, не ниже. Красноватый оттенок и дитолу при дает большое присутствие свободного фенола.
Бакелиты ~ С12НПО2 (формула условна); пс другим источникам — С14Н4О3 — искусственная смола, получаемая конденсацией фенола с избытком формальдегида в присутствии щелочного ка тализатора (аммиака), В пиротехнических составах,- как и идитол, применяется в качестве связующего горючего. Бакелиты устойчивы к химическим воздействиям, являются хорошей защитой активных металлических порошков в смесях с нитратами и хлоратами. Бакелит «А» размягчается при температуре 75-1ОО°С, он хорошо растворяется в этиловом спирте. Если нагревать бакелит «А» выше 100°С, он переходит в форму «В». С дальнейшим повышением температуры до 180°С его форма меняется и переходит в бакелит «С». Бакелит «С» — неплавкое вещество, не размягчается, не растворим в большинстве органических растворителей, очень устойчив к химическим воздействиям и обладает большой механической прочностью. Мы работаем с бакелитом формы «А» в виде спиртового лака. Если составы с примесью бакелита «А» нагреть в спрессованном виде до температуры 150-180°С, то бакелит «А» через форму «В» перейдет в форму «С», чем весьма укрепит наше изделие не только химически, но и механически. Надо учесть, что изделия, изготовленные таким методом, будут очень стойки и к лучу огня, то есть возгорание таких изделий потребует или специального зажигательного состава, или более мощного начального импульса. Иногда в изделиях требуется не только зажигательный состав, но еще и переходный — от зажигательного к основному. Но об этом речь впереди. Бакелиты применяются в термитно-зажигательных смесях, в осветительных составах. Бакелит употребляется в некоторых составах цветных звездок для «бураков» и «люстку гелей». При работе с бакелитами обязательно проветривать помещение. Бакелиты токсичны.
Канифоль — C2()H.WO — естественная смола, получаемая из древесины и смолы хвойных деревьев, обработанная высокой температурой;, низкая температура плавления канифоли (немногим выше 65°С) не дает возможности получать тонкие порошки и изучить все ее возможности. Главной составной частью канифоли является ненасыщенная абиетиновая кислота (С20Н30О2). Плотность = 1,0-1,1 г/см3. Канифоль растворима в этиловом спирте, эфире, бензоле, частично в бензине; при нагревании растворяется в олифе. В качестве горючего канифоль применяется в составе павильонного дыма. В качестве связующего канифоль очень редка. Большая концентрация пыли канифоли в воздухе взрывоопасна. Канифоль не вредна, однако при работе с канифолью в помещении надо надевать респиратор или ватно-марлевую повязку (ибо канифоль забивает дыхательные пути, покрывает пленкой слизистую носа и глаз). После работы обязателен душ.
Резинаты — получаются от сплавления солей металлов с канифолью, вернее, с абиетиновой кислотой. Так, резинат кальция получается сплавлением канифоли с гашеной известью при температуре 230-240°С, после чего получается резинат кальция — (С19Н2дСОО)2Са. Однако эта формула берется только для расчета при составлении новых смесей, новых рецептов. Резинаты бывают не только кальция, но и стронция, и калия, и других металлов. Плотность резината кальция =1,2 г/см3; условная молекулярная масса — 643; за счет сгорания 1 г кислорода резината кальция сгорает 0,61 г. Если рассмотреть элементарный состав резината кальция, то увидим, что он содержит: углерода — 75 атомов, водорода — 9 и кислорода — 10 атомов. Резинат кальция растворяется в бензине или в смеси бензина со спиртом 1:1. Резинат кальция в пиротехнических составах дает яркое белое пламя. В нашем производстве почти не употребляется. Из других резинатов интересен резинат стронция (Sr2OH30O2). Смеси с резинатом стронция дают чистое красное пламя. Применяется в оборонной промышленности, в ракетной и космической технике. В иностранной литературе есть несколько рецептов с резинатами, но для нас они непригодны из-за своей высокой стоимости. Резинаты почти безвредны, при работе с ними надо только защищать органы дыхания от пыли. Для этого годится даже ватно-марлевая повязка или простейший респиратор «Лепесток».
Олифа натуральная — С16Н28О2 — вязкая жидкость бурого цвета. Получают олифу продуванием воздуха через нагретое до 160°С льняное или конопляное масло. В малярном производстве в олифу добавляют различные добавки — «сушители», способствующие скорейшему высыханию олифы. В пиротехнике такие добавки невозможны. У нас употребляется чистая олифа. Для некоторых составов можно применять раствор канифоли в олифе, но только в тех рецептах, где указана канифоль в качестве компонента со своим процентным соотношением. Олифа не ядовита.
Декстрин — С6Н10О5 — клей растительного происхождения. Получен из крахмала путем нагревания с разбавленными кислотами. Желтый порошок, легко растворяется в горячей и холодной воде, как клей готов к употреблению без предварительной подготовки. Как горючее-связующее — улучшает чистоту пламени в цветных огнях. Продукт недорогой, безвредный. В пиротехнических составах широко применяется и как компонент, и как клеящее вещество. Клей можно получить из кукурузы, из картофеля. Это продукт расщепления переменного, еще не точно изученного в деталях, состава, который образуется в результате разложения крахмала под действием ферментов и высокой температуры (180-200°С) или кислот. Декстрин состоит из точно не известного количества молекул глюкозы, и потому его формула является приблизительной, но она хороша для подсчета при расчете в рецептах и пиротехнических смесях. Однако надо помнить, что декстрина есть по меньшей мере две разновидности: декстрин «а» — (СвН10О6)5 и декстрин «б» — (с,н10о,).:
Шеллак — С16Н24О5 — естественная смола, аморфная твердая коричневая чешуйка. В России не добывается. Покупаем мы ее в странах Юго-Восточной Азии. Хорошо растворяется в спиртах, ацетоне, эфире, скипидаре. В воде не растворяется, В пиротехнических составах употребляется в виде лака, лачного раствора в спирте. Применим и в спекаемой смеси с окислителем с последующей размолкой двухкомпонентного состава до необходимой величины частиц. Так, для пламенных составов красного цвета шеллак смешивают с нитратом стронция и спекают в открытом виде до однородных кусков неправильной формы с последующим их измельчением. Шеллак в России дефицитен и дорог, однако малодымные и химически стойкие составы цветных огней оправдывают его применение в пиротехнических составах. Шеллак безвреден.
Смола ФР-12 — фенольно-резерциновая, применяется в качестве горючего-связующего, цемен-татора в газообразующих составах, обязательно с отвердителем-параформом. Активное горючее с нитратами, скорость горения составов со смолой ФР-12 близка к скорости горения дымного черного пороха. Работа со смолой требует дополнительного оборудования из-за вязкости смолы, а при добавлении параформа — для быстрого высыхания. При работе со смолой ФР-12 рекомендуются респираторы из-за ее летучих свойств в смесях с параформом.
Сырой буроугольный воск — озокерит, «мон-тан воск», «горный воск» — продукт перегонки бурого каменного угля. Применение — самое широкое в качестве горючего-связующего в составах цветных огней и различных составах белого дыма. Из-за низкой температуры плавления (около 75°С) горный воск при размалывании летом может спекаться в монолит прямо в шаровой мельнице. Поэтому его рекомендуется размалывать зимой, при низких температурах. Хорошо размалывается до тонкого порошка, не гигроскопичен, хранится без слеживания и кристаллизации, безвреден, не опасен. При размолке, просеивании и работе с пылящими составами защита органов дыхания — простой респиратор-«Лепесток» или марлевая повязка. Горный воск не растворим в воде, легко растворяется в спирте, бензине, ацетоне. Употребляется в виде порошка с последующим вводом растворителя, покрывает надежной прочной пленкой отдельные компоненты состава, а при среднем давлении запрессовки цементирует пиротехнические смеси.
Катализаторы — это элементы, а чаще химические вещества, которые вводятся в пиротехнические составы для ускорения горения этих составов. Проблема катализа при горении пиротехнических составов еще полностью не разрешена. Опыты в лабораторных испытаниях показали, что катализаторы наибольшее влияние имеют в пиротехнических смесях с низкой температурой горения. С повышением температуры горения составов, как правило, повышается и внутреннее давление продуктов сгорания, а при таких условиях роль катализатора будет уменьшаться. Во многих пиротехнических составах они не употребляются вообще, так как горение поддерживается на высоком уровне за счет сгорания компонентов: окислителя и горючего, дополнительных специальных химикатов; солей, окрашивающих пламя в заданный цвет; горючих, образующих много дыма или много газов. Многие катализаторы-химикаты вводятся в составы не в качестве катализаторов, но выполняют эту функцию параллельно со своей основной задачей как равноправного компонента. Об этих химикатах и пойдет речь ниже.
Аммоний хлористый — NH4C1 — нашатырь. Технический аммоний хлористый весьма гигроскопичен. В пиротехнике употребляется «аммоний хлористый» — «чистый». Это дымообразующее ■ горючее, способное к обменным реакциям в смесях с хлоратами, но в присутствии с другими компонентами аммоний хлористый более химически стоек. Основное применение: в различных дымовых составах с низкой температурой горения, где он
Катализаторы выполняет и роль катализатора. Аммоний хлористый применим и в составах цветных огней, где также выполняет функции катализатора, так как цветные звездки, например, горят в воздухе. Аммоний хлористый не токсичен.
Двуокись марганца — МпО2 — пиролюзит. Черный или коричневый порошок; как катализатор снижает температуру горения хлоратов на 8, если добавить в пиротехнический состав всего 5% от общего объема состава. Токсичен. Ядовит. Резко повышает чувствительность пиротехнических смесей с хлоратами к механическим воздействиям. Смешивать такие составы надо обязательно в спиртововодной среде. Готовое изделие просушить. Молекулярная масса МпО2 = 87, плотность = 5,0 г/см3, тем-пература плавления больше либо равна 500°С, активного кислорода в составах имеет 37%. Используется в термитных смесях. При работе с двуокисью марганца пользоваться противогазом, резиновыми перчатками. После работы обязателен душ. .
Окись кобальта — Со203 — черно-серые кристаллы — чистый катализатор, по своим свойствам и характеристикам в пиротехнических составах производит такие же действия, как и двуокись марганца. Воздерживаются от смесей с хлоратами, особенно в сухом виде. Токсичен, ядовит. Все меры предосторожности при работе с окисью кобальта, как и с предыдущим химикатом (Мп02).
Соединения хрома — (NH4)2Cr2O7 — бихромат аммония; СгО3 — трехокись хрома; К2СгО4 — хромат калия — применяются как катализатор в газообразующих и искристых составах с нитратом аммония. Соединения хрома крайне токсичны, вызывают аллергию, особенно хромат калия К2СгО4; по этим причинам в нашем цехе рецептов и изделий с соединениями хрома мало. Людям с повышенной чувствительностью и больным аллергией работать с этими солями-окислителями, катализаторами не рекомендуется — может наступить шоковое состояние.
Железистосинеродистое железо (берлинская лазурь, прусская синька, «милори») — Fe4[Fe(CN6)]3 — порошок темно-синего цвета; не летуч, гигроскопичен —- является катализатором в искристых и газообразующих составах, в некоторых фейерверочных изделиях. Не токсичен. Защита от пыли — ватно-марлевая повязка.
Пламягасители обычно в пиротехнических составах применяются при производстве дымов различного цвета. Хорошими пламягасителями зарекомендовали себя углекислые соли: мел — СаСО3; углекислый магний — MgCO; фторид бария — BaF2 — он же является и флегматизатором — химикатом, препятствующим слеживанию составов и перекристаллизации химикатов в составах при их длительном хранении; ортофосфат кальция — Са(РО4)2. Продукты, выделяющие при своих реакциях углекислый газ — СО2,— являются пламягасителями. Как правило, все эти соединения — при работе с ними, при контакте — не токсичны. Но продукты их горения ядовиты. Это надо помнить всегда, когда применяются изделия с добавками пламягасителей в помещениях. Исключением может быть павильонный дым — состав, где СО нейтрализуется, соединяясь со свободным хлором, получаемым от сгорания бертолетовой соли и аммония хлористого.
Двухкомпонентные смеси и их значение при построении пиротехнических рецептов и изделий из них
Ранее мы выяснили, что для любой реакции, которая «пойдет вправо», то есть будет реагировать, будет гореть, нужны окислитель и горючее в обязательном порядке. Есть исключения, когда горючие без окислителей горят на воздухе. В таких случаях горючие берут кислород для своего окисления из атмосферного воздуха. Нам же необходима смесь, которая, сгорая, давала бы нужный эффект, заранее задуманный и рассчитанный. Все пиротехнические рецепты построены так, что сначала подбирают окислитель и горючее, а затем, вводя специальные добавки, добиваются нужного эффекта, то есть основой всех пиротехнических изделий является двухкомпонентная смесь. Если изделие сложное, то в одной пиротехнической смеси могут быть две и даже больше двойных смесей. Ниже, когда будет речь идти о тех или других рецептах сложных изделий, мы еще вернемся к этому вопросу и поговорим об этом подробнее. При знакомстве с окислителями одним из первых был нитрат бария Ba(NO3)2. Мы хорошо ознакомились с его свойствами, мы его знаем и непосредственно по производству, где его называем барием азотнокислым. А при знакомстве с горючими одним из первых был активный металл — магний (Mg). На основе этих двух компонентов мы попробуем сделать пиротехническую смесь и посмотреть, что из этого получится. Итак, у нас на рабочем столе лежат соль бария — окислитель и порошок магния — горючее. Самый тонкий порошок магния, которым пользуются кинопиротехники, № 4; он намного крупнее зерен-частиц соли бария азот
нокислого. Но у них и плотность довольно разная,
поэтому в смеси, при небольшом начальном импульсе
они реагируют хорошо и устойчиво. На этих двух
компонентах-химикатах можно построить много ре
цептов:
Ba(NO3)2+ Mg: а) 68% +32%; б) 60% + 40%; в) 50% + 50%; г) 45% + 55%; д) 35% + 65%; е) 31,7% + 68,3%.
В данном случае мы убавляли окислитель — (Ba(N03)2) и увеличивали процентное количество магния (Mg), причем увеличивали Mg довольно большими дозами и соответственно такими же дозами уменьшали количество Ba(NO3)2- Вы не могли не заметить, что, например, между первым и вторым рецептами, количество Mg увеличилось сразу на 8%, а количество Ba(NO3)2 на столько же уменьшилось. Каждый из нас, без посторонней подсказки, знает, что между этими двумя — первым и вторым рецептами находится еще много возможных вариантов рецептов пиротехнических смесей. У нас ЄСТЬ ВОЗІЇ можность брать не только по одному из этих 8%, но s и десятые доли процента, как это показано в последнем рецепте. Именно здесь и заложены те возможности влияния на пиротехнические изделия, на их заданность, которые мы и используем в своих целях при разработке новых рецептов и изделий. Надо заметить, что с увеличением количества магния и
_________________ ПИРОТЕХНИК 1 уменьшением количества нитрата бария будет воз-растать яркость вспышки, скорость горения в та-
-ких смесях не уменьшится. Мы говорили об увеличении количества магния в этих смесях, но если Ї прочитать эту шкалу рецептов снизу вверх, то получится наоборот, количество магния будет уменьшаться. В таком случае яркость вспышки будет уменьшаться, потому что свечение пламени в таких смесях дают порошки активных металлов. Соль бария, в данном случае — нитрат бария Ba(NO3)2, будет только способствовать светимости пламени. Вспышки всех этих составов будут яркими, и цвет у них будет белый. Мы же знаем, что соли бария (Ва) окрашивают пламя в зеленый цвет, значит, пламя магния •преобладает над пламенем соли бария. Примерно так же будут выглядеть смеси с алюминием (А1), цирконием (Zr) и титаном (Ті).
Для осветительных изделий, для вспышек и имитаторов, для всех пиротехнических эффектов от нас, пиротехников, требуется, как правило, видимость этого эффекта, чтоб его можно было зафиксировать в -кино. На этой основе и разрабатываются все рецепты для кинопиротехники. Мы знаем, что таблица Менделеева содержит в своем составе около 105 элементов. Соединений различных элементов очень много, а мы познакомились с 35—50 из них. Возмож- | ности расширения применения других химикатов да- ;1 леко не исчерпаны в пиротехнике. В качестве окис- , лителей есть большой запас химикатов, а в качестве горючих мы ограничены, в основном, стоимостью этих химикатов и элементов. Так, из горючих металлов у нас употребляются алюминий и магний, а также сплав этих двух металлов. При работе, при разработке новых рецептов следует исходить из тех материалов, которые легко достать, — купить за небольшое время и за небольшие деньги. Причем вторая причина наиболее весома. Каждый пиротехник должен стремиться к тому, чтобы сделать пиротехническое изделие, отвечающее требованиям, но более дешевое, несложное по изготовлению и безопасное не только по применению, но и по своему токсичному действию на людей й животных. Компоненты изделий должны быть подобраны так, чтобы избежать по возможности нежелательного излучения в других спектрах или частях спектра. Элементы, получающиеся при горении состава, должны быть такой окраски, которая задумана именно для этого изделия. Они должны быть летучими и уже при температуре в 1000°С полностью переходить в газообразное состояние. Этим требованиям полностью отвечают хлораты щелочных металлов. На второе место можно поставить нитраты, которые имеют температуру плавления и перехода в газообразное состояние 1200°С.
О составах цветных огней в пиротехнических изделиях со многими необходимыми компонентами.
Их характеристики. Составы цветных пиротехнических изделий.
Требования техники безопасности при их изготовлении и использовании
Составы сигнальных и осветительных огней обычно содержат компоненты:
а) окислители;
б) горючие;
в) соли, окрашивающие пламя, свечение;
г) хлорсодержащие соединения, улучшающие окраску пламени;
д) неорганические горючие (порошки металлов, повышающие силу пламени, свечения).
Бывает, что окислитель хорош тем, что он является еще и красителем пламени, но он гигроскопичен. Составы с таким окислителем хранить долго нельзя — начинают разлагаться порошки металлов, и изделия приходят в негодность. В таких случаях ищут и находят другой компонент — негигроскопичный, богатый и хлористым содержанием, и кислородом. Однако надо помнить и о цвете пламени, значит, надо в рецептуру добавлять еще один компонент — для окраски пламени. Негигроскопичными, богатыми хлорсодержащими и содержащими кислород являются соли калия (К). Но соли калия дают белое пламя при своем горении, а необходимо получить цветное. Здесь нам помогут соли, окрашивающие пламя, свечение нашего состава, в небольших количествах.
Очень хороши в таких смесях органические горючие, дающие бесцветное пламя, если горят одни; при горении других компонентов эти горючие усиливают цвет того красителя пламени, который является главным, хотк его в составе и не так уж много. Органические горючие, дающие бесцветное пламя: сера (S), водород (Н), окись углерода (С02) — при горении на воздухе, при атмосферном давлении. В дневное время при сжигании этих горючих их пламя не видно, даже если чистого данного вещества содержится только 50% от всей массы вещества. При этом рассчитывать на полное сгорание веществ не приходится. Мы уже говорили о введении новых химикатов-компонентов в пиротехнические составы по мере их промышленного изготовления и пытливости пиротехников-предшественников. Вот такой пример: осветительный состав времен Первой мировой войны белого цвета: нитрат бария — 76%; алюминиевая пудра — 10%; порошок алюминия № 4 — 8%; сера — 4%; масло касторовое — 2%.
В то время этот рецепт военные пиротехники держали в большом секрете. Можно здесь же рассмотреть этот рецепт с другой стороны: нитрат бария, азотнокислый барий (Ba(NO3)2) должен при таком преобладающем, доминирующем присутствии окрасить пламя в зеленый цвет, сера (S), как органическое горючее, подчеркивающее только чужое пламя, должна была подчеркнуть пламя нитрата бария. Но этого не произошло из-за того, что алюминия, горючего неорганического, в общей сложности в данном рецепте находится 18%. Яркость его пламени начисто забила цвет пламени бария нитрата. Дальнейшие предложения и искания пиротехников показали, что если в этот состав ввести фто ристый натрий — NaF, криолит — Na3AlFe или даже нитрат калия — KNO3, свечение такого состава поднимется на 15-20%. О белых огнях и их составах, которых наибольшее количество из всех других сейчас разработано, поговорим отдельно. Наша задача в данном разговоре — цветные огни, а старый рецепт мы привели в качестве примера, насколько возросли возможности пиротехники за такое исторически короткое время.
В пламенных составах желтого цвета наиболее часто употребляют соли натрия, несмотря на их гигроскопичность. Самой ходовой из них является нитрат натрия — NaNOs. В цеховой книге рецептов можно найти много рецептов на основе нитрата натрия, и это несмотря на то, что книга является новой. В старой книге, которая, к сожалению, кем-то унесена и не возвращена, можно было проследить эволюцию отработки пламенных составов желтого, да и не только желтого, а и других цветных огней. Вновь начатая книга регистрации пиротехнических рецептов этой эволюции не отображает, но для сравнения можно посмотреть рецептуру в книге великого русского пиротехника П.С. Цытовича «Опыт рациональной пиротехники», изданной в 1894 году. Правда, уже тогда основу желтопламенных пиротехнических составов являл натрий азотнокислый. Вот, к примеру, состав для звездок желтого цвета: нитрат калия — 37%; оксалат натрия (еще он называется щавелевокислый натрий) — 30%; магний №4 — 30%; смола — 3%.
В этом рецепте нитрат калия (KN03) является окислителем дополнительным, а оксалат натрия (NaC2O4 H2O) выполняет две функции — и носителя кислорода, и соли, окрашивающей пламя в нужный нам цвет. Магний при сгорании дает яркость пламени, а смола является цементатором и вместе с магнием дополнительным горючим.
Второй рецепт желтого пламени: NaNO3 — 74%; S — 8%; Al — 18% без цементатора; значит, он предназначен для сжигания не в спрессованном виде, а в порошке.
Такие порошкообразные составы предназначены для «фигурных» свечей. В магазинах, где продают пиротехнические изделия, «фигурные» свечи иногда называют «контурными» («контурными» их иногда называют и пиротехники младшего поколения). Этот рецепт показателен тем, что в нем 74% его массы составляет нитрат натрия. На долю двух горючих — серы (8% ), которая в этом рецепте усиливает, подчеркивает цвет и силу горения нитрата натрия, и алюминия (18%), самого настоящего горючего, дающего основную часть пламени, свечения, приходится всего 26% общего объема состава. Еще один типичный рецепт желтопламенного состава; он предназначен для изготовления бенгальского огня и показывает доминирующую часть нитрата натрия в своем составе: NaNO3 — 63%; S (сера) — 26%; С (уголь древесный) — 11%; идитол (или декстрин) — 2%.
Этот рецепт используется в консистенции густой сметаны, состав его должен прилипать к
ffMWm'LWIHIM ■ К ■ VTT rIMKPWMMI—MHMWMIU ІЛ Mnv ШИтМММИМШЙМИП Г >rminWWl,tWMrtW.-ir
отрезкам проволоки и потому разводится на воде или на спиртово-водной смеси, где цементатор — идитол (С13Н12О2) или декстрин (С6Н10Ое). Эти вещества являются, в основном, цементаторами, хотя при высыхании в составах, как было сказано ранее, выступают и дополнительными горючими. Здесь стоит обратить внимание именно на это замечание, что цементаторы, как бы ни было мало их количество в общей массе пиротехнического состава, являются горючими, и этим нельзя пренебрегать в дальнейшем, при построении новых рецептов. Как бы ни было мало их количество, для того, чтобы реакция была полной, качественной, шла до конца, им, этим горючим—цементато-рам, необходим кислород окислителя.
Красное пламя при горении дают соли стронция — Sr. Пиротехники исключают лишь фторид стронция — SrF, так как этот химикат дает не чистое красное пламя, а окрашивает его в желто-зеленый цвет, и поэтому в пиротехнических смесях не пригоден. Лучшим красителем пламени в таких смесях является монохлорид стронция — SrCl. Этот химикат за счет хлора горит лучше и окрашивает пламя в более интенсивный красный цвет. Однако хлорид стронция весьма гигроскопичен, уже при относительной влажности окружающего воздуха, 65% хлорид стронция превращается в мокрую соль — SrCl H2O. Наиболее удобными и наиболее часто употребляемыми в пиротехнических смесях красного пламени в наших условиях являются нитрат стронция — SrNO3, оксалат стронция или щавелевокислый стронций — SrC2O4, а также, правда, реже, стронцианит, карбонат или углекислый стронций — SrCO2. Необходимо заметить, что в составы красного пламени, в большинство их, вводят хлорат калия, бертолетову соль (КС1О3) и перхлорат калия (КС104). Как известно, эти соли калия дают бесцветное мощное собственное пламя, негигроскопичны, богаты хлором и кислородом, легко отдают кислород при реакциях. Как правило, к этим солям калия добавляют красящую соль. В данном случае добавляют соли стронция. Надо заметить, что соли калия после сгорания дают много шлака, а это не всегда хорошо. Рецептов на этих основах много, и на них мы не будем останавливаться очень подробно. С точки зрения пиротехников-теоретиков, как у нас в стране, так и в зарубежной литературе, все большее применение в рецептах пламенных составов, в том числе и красного цвета, находит прогрессивный химикат перхлорат аммония —■=-NH4C1O4. Есть и уже применяется на практике рецепт красного огня с перхлоратом аммония: перхлорат аммония — 40%; нитрат стронция — 35%; уротропин — 15%; тиомочевина — 5%; идитол — 5%.
Чистота цвета пламени этого состава (92%) —* очень высокий показатель среди пламенных пиротехнических изделий. С точки зрения кинопиротехники этот состав не всегда, вернее, не во всех изделиях красного пламени удобен из-за того, что при горении перхлората аммония образуется очень большое количество дыма. В факеле такое количество дыма почти неприемлемо. Если факелы красного огня изготовлены по этому рецепту, — на них надо
ПИРОТЕХНИК ставить особую отметку — «образует много дыма, вблизи камеры обращаться осторожно». В «пожарах» же такой факел будет находкой. Хороши звезд-ки для «бураков» и «люсткугелей» из такого состава, потому что ночью нужно свечение, дым в воздухе ночью не очень заметен. Выдержал много лет без изменений и такой состав красного огня, отработанный в нашем цехе: нитрат стронция — 65%; порошок магния №4 - 11%; уротропин — 19%; озокерит — 5%; масло веретенное — 0,1%.
Здесь, наверное, надо обратить внимание на довольно большое количество уротропина (C0H12N4) в этом составе. Такое его количество оправдано тем, что уротропин — хорошее горючее с бесцветным собственным пламенем, малодымен, при горении подчеркивает, усиливает пламя того цвета, который преобладает в составе. В нашем случае нитрата стронция — Sr(NO3)2 — 65%, и он является окислителем и красящей пламя солью одновременно. Порошок магния, составляющий 11%, усиливает свечение состава при горении, озокерит — цементатор и горючее, так же, как и масло, растворяющее озокерит, а при высыхании оставляющее озокеритовую пленку в изделии, защищающую состав от проникновения влаги, а значит, и от коррозии порошка магния.
По литературным данным, очень хорошие цвета зеленого пламени дает при своем сгорании таллий — Т1. Но это очень редкий химический элемент и потому очень дорог. Относительно таллия — поверим литературным сообщениям,.возьмем себе на заметку и, при случае, может быть, попробуем его в пиротехни-
ческом составе. А пока все пиротехники смеси для получения зеленого пламени приготовляют на основе солей бария (Ва). Составы зеленого огня с солями бария разрабатываются, как правило, с отрицательным кислородным балансом (КБ), потому что при наличии лишнего кислорода может протекать реакция разложения хлорного бария — ВаС12 с образованием окиси бария ВаО2, а окись бария и горит плохо, и плохо окрашивает пламя. Фторид бария — BaF2 — для получения зеленого пламени в пиротехнике не применяется, так как его пламя смещено в желтую часть спектра. Очень хорошие цвета при своем сгорании обеспечивает хлорат бария. Но этот химикат у нас не применяется, так как его смеси весьма чувствительны и опасны при обращении. Перхлорат бария — очень гигроскопичная соль, а потому также не применяется в нашем производстве. В пиротехнических изделиях наибольшее применение и распространение получили две соли бария: нитрат бария — Ba(NO3)2 — употребим в большем количестве и углекислый барий, карбонат бария — ВаСО2 — в меньшем количестве. Именно они и дают зеленый цвет в пламенных пиротехнических составах. В качестве основных окислителей в таких составах чаще всего бывают: перхлорат калия — КС1О4, хлорат калия — КСЮ3 и перхлорат аммония — NH4C1O4. При этом хлораты и перхлораты несут двойную функцию: и как горючие, по богатству кислорода и легкому его отделению; и как хлорсодержащие соли, усиливающие пламя и его цвет, сами не являясь красящими пламя веществами. Вот несколько из множества рецептов составов зеленого пламени.
I. Нитрат бария — 40%; магний (МПФ-4) — 28%; гексахлорбензол — 30%; олифа — 2%.
П. Нитрат бария — 59%; магний № 4 — 19%; поливинилхлорид — 22%.
Ш. Нитрат бария — 45%; перхлорат калия — 16%; магний порошок № 4 — 26%; гексахлорбензол — 7%; окись меди (СиО) — 2%; олифа — 2%.
IV. Нитрат бария — 23%; перхлорат аммония — 49%; уротропин — 18%; идите л — 7%; тиомочевина — 3%; ферроцен — 0,2% сверх 100%.
Состав рецепта IV не сильно чувствителен к механическим воздействиям и имеет чистоту цвета около 90%. Зеленую окраску пламени можно получить и вводом в составы соединений бора (В), однако чистота цвета пламени с его добавками бывает недостаточной, бледной. Зеленый окрас пламени дает и медь, и ее соли на горелке, но в пиротехнических смесях в любых сочетаниях и с любыми химикатами пиротехники-практики не получили еще удовлетворительного зеленого пламени. Терять надежды не стоит. Химическая промышленность вырабатывает много новых химических соединений, поэтому новому поколению пиротехников может быть удастся найти хорошие сочетания и меди, и бора для зеленопламенных составов.
Характерные яркие линии в синей части спектра получены при сжигании индия (In) и его соединений. По теоретическим расчетам и утверждениям химиков-аналитиков, этот элемент периодической таблицы Менделеева был бы идеальным красителем для пламенных смесей голубого огня. Нам же, практикам, да еще при работе в кино, остается только верить теоретикам. Проверить на практике возможности индия мы не можем — нет его в нашем распоряжении. Высока его стоимость, редок на земле этот элемент. Синее пламя получают на основе горения монохлорида меди (CuCl). В качестве красителей пламени в пиротехнике используют малахит (CuCO3Cu(OH)), сернокислую медь (CuCNS) и другие соединения меди, а также металлические опилки меди, прокипяченные в масле. Соединения меди сообщают пламени нечистую зеленую или синюю окраску, но всегда надо помнить о том, что смеси с медью для получения синего огня надо составлять: с большим дефицитом кислорода, с избыточным количеством хлора и чтобы температура горения смеси голубого огня не превышала 1000-12О0°С.
В качестве отправной точки можно попробовать такой рецепт для получения голубого огня: хлорат калия — 46%; окись меди (СиО) — 15,5%; нитрат калия — 15,5%; сера — 23%.
Здесь надо сказать о том, что некоторым цветнопламенным смесям не повезло. Тем самым, о которых мы сейчас говорили: синему, голубому и фиолетовому. Пиротехники кино, где рецептура изделий зависит от пленок, менее всех виноваты в таком положении. Однако есть и другие отрасли, где пиротехники просто обязаны были давно найти безопасные и дешевые, а главное, хорошие чистопламенные смеси этих огней. Цветам: красг ному, зеленому и желтому в этом отношении повезло больше. А вот состав синего огня: хлорат калия — 61%; горная синь (2CuC03Cu(OH)2)— 19%; сера — 20%.
В данном составе сера взаимодействует с хлоратом калия с выделением свободного хлора, и в присутствии серы монохлорид меди не образуется. Если же в составе образуется монохлорид меди (CuCl) как промежуточный, то синего пламени добиться будет невозможно. Тем не менее, можно без натяжек говорить, что со времени выхода в свет в 1894 году книги Цытовича мало что изменилось в изготовлении огней фиолетового, голубого и синего.
Вот типичные составы цветных огней по данным некоторых зарубежных публикаций, и опять это цвета трех наиболее часто разрабатываемых смесей: красного, зеленого, желтого. •
|
Компоненты смеси |
Содержант, % | |||||
|
составь» красного огня |
составы зеленого огня |
составы желтого огня | ||||
|
Магний |
40 |
29 |
16 |
26 |
9 |
26 |
|
Нитрат стронция |
30 |
34 |
- |
- |
- | |
|
Нитрат бария |
- |
- |
59 |
45 |
• |
29 |
|
Оксалат бария |
- |
• . |
- |
- |
17 |
13 |
|
Перхлорат калия |
20 |
29 |
- |
16 |
50 |
23 |
|
Г ексахлорбензол |
5 |
4 |
21 |
7 |
9 |
5 |
|
Медный порошок |
- |
- |
2 |
• |
- | |
|
Окись меди |
- |
- |
- |
2 |
- |
- |
|
Масло |
- |
2 |
2 |
2 |
3 |
2 |
|
Асфальт |
5 |
- |
- |
- |
12 |
- |
|
Силсоний * |
- |
2 |
- |
2 |
- |
2 |
*- силсоний — фирменное связующее вещество, другими сведениями о нем автор не располагает.
О составах белого огня
Подбор химикатов для изделий. Требования техники безопасности при изготовлении смесей белого огня и при их применении
Существует очень много комбинаций химикатов, при смешении которых получается белое пламя. Рецептам белого цвета придавали значение всегда потому, что это не только сигнальные огни, видимые на большом расстоянии в ночное время, но это и осветительные составы, в том числе и боевые, применяемые в военное время. Мы в кинопиротех-нике применяем их с той же целью: это осветительные факелы различного назначения, диаметра, времени горения и вспышки. В качестве горючего в таких смесях берут один из обычных и постоянных, опробованных легких металлов — алюминий или магний, В качестве окислителей — нитраты и хлораты щелочных металлов. Из других компонентов можно выбрать химикаты, которые при своем сгорании дают белое пламя: сурьма чистая (Sb), антимоний сурьма трехсернистая (SbS3(Sb)), сера (S), нитрат калия (KNO3), нитрат бария (Ba(NO3)2), фторид бария (BaF) и другие химикаты. Вот один из старых рецептов: нитрат бария — 56%; нитрат калия — 11%; фторид бария — 6%; порошок алюминия № 4 — 19%; сера — 8%.
Этот рецепт использовали в осветительных бомбах во время второй мировой войны почти все воевавшие страны. Компоненты, входящие в этот состав, недорогие, доступные. Производство не опасное. Можно было делать замесы на 1000 кг одновременно. Когда стали отмечать крупные победы на фронтах Великой Отечественной войны производством салютов, фейерверочное искусство получило дополнительный толчок в своем развитии. Требовались новые красивые изделия. Пиротехники начали искать новые сочетания химикатов в своих составах. Вышеприведенный состав не устраивал, потому что он не обеспечивал яркого пламени белого цвета — нитрат калия дает розоватый огонь, а нитрат бария — зеленый. И хотя присутствует много алюминия — 19%, пламя нужной яркости именно белого цвета не получалось. Однако состав этого пламени был тогда государственной тайной. В результате долгих опытов были найдены другие сочетания химикатов, обеспечивающих при горении белое пламя. В качестве главного окислителя взяли перхлорат аммония (NH4C1O4), к нему добавили горючие с низкой температурой кипения: уротропин (C6Hl2N4) и идитол (С13Н12О2); небольшая добавка, всего 3%, из антимония (SbS3) хорошо усилила свечение смеси и за счет цветов и оттенков в пламени белого огня. Ниже мы приводим полностью рецепт этого сочетания химикатов: перхлорат аммония (NH4C1O4) — 67%; уротропин (C6H12N4) — 17%; идитол (С13Н12О2) — 3%; антимоний — сурьма трехсернистая — 3%.
Итак, казалось бы, все хорошо. Но так не бывает. Этот состав, обеспечивающий при сгорании отличное белое пламя, выделяет очень большое количество дыма. Такая смесь хороша для фейерверочных изделий, сжигаемых на воздухе, ночью на стадионах и в парках. В ночных условиях дым рассеивается в воздухе позже сгорания звезд ок, а эффект от фейерверка великолепен, так как яркость, сила света и белый
О составах белого огня________________________ цвет пламени позволяют видеть его на больших расстояниях. Вот несколько рецептов белого огня из зарубежной специальной литературы:
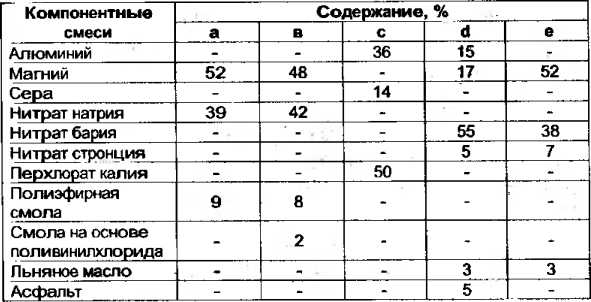
В этих рецептах нет перхлората аммония, столь полюбившегося нам по предыдущему рецепту, который выделяет очень много дыма. Здесь мы видим присутствие легких металлов — магния и алюминия, которые при своем горении выделяют тоже очень много дыма; в наличии и цветнопламенные нитраты щелочных металлов, и перхлорат калия, которые, увы, также не бездымны. Но это не значит, что мы должны пренебрегать такими смесями при потребностях смесей белого пламени. Более того, при удобном случае надо каждую из этих смесей попробовать, посмотреть самому, сравнить с другими и уже потом делать личный вывод, составлять собственное мнение об эффекте, полученном при сгорании этих составов, и применять их на практике, которая у пиротехника может составлять всю жизнь.
До этого момента мы говорили о простых рецептах и смесях, которые представляли собой механические смеси двух или нескольких химикатов. Есть несколько усложненный метод получения некоторых компонентов для пиротехнических изделий. Ведь пиротехник, особенно кинопиротехник, — всегда экспериментатор, всегда в поиске. Готовые рецепты взять и изготовить по ним какое-то изделие легче, чем искать новые сочетания химикатов для решения конкретно поставленной задачи. Но чем труднее задача — тем интереснее ее решать, и еще большее удовлетворение получаешь, когда эта задача решена положительно. Конечно, для этого должны быть все слагаемые: химикаты, инструменты, приспособления, оборудование. Главное — иметь желание экспериментировать, заниматься лабораторно-исследовательской работой.
При этом необходимо всегда иметь при себе тетрадь, блокнот, а лучше журнал для записи результатов. Ученые люди говорят, что даже отрицательный результат — это тоже результат. Главное при исследовательской работе в пиротехнике — не увлекаться количеством состава, количеством смеси. При работе с незнакомыми химикатами и материалами необходимо принимать все меры предосторожности и безопасности, как в отношении себя лично, так и других людей, помещения, оборудования. При экспериментах надо в обязательном порядке работать за щитком или в защитных очках и перчатках, а в некоторых случаях — надевать противогаз. И опять о количестве: навески экспериментальных составов
не должны превышать нескольких граммов, особенно, если составы химикатов дают чувствительные смеси к механическим воздействиям. В помещении, где проходит не только экспериментальная работа, но даже работа со знакомыми материалами и изделиями, ничего лишнего, не относящегося к данной работе, к данному изделию, не должно быть.
Мы привыкли к тому, что яркость пламенным составам придают легкие металлы: Al, Mg, W, Ті и другие. Однако на практике может оказаться так, что нет этих металлов, порошков нужного калибра или несовместимость химикатов не позволяет вводить порошки легких металлов, а эффект в кинокартине нужен. Не серийное изделие — преходящее, вспышка красного, зеленого, желтого огня. В таких случаях пользуются смесью: нитрата калия — 50%; серы — 50%.
Эту смесь нагревают в посуде до полного спекания, до однородности, постоянно помешивая, чтобы не было подгорания. Когда смесь получит вид однообразной массы желто-серого цвета^ — надо снять ее вместе с посудой с нагревателя, высыпать на чистый картон или фанеру и дать остыть. Получатся бесформенные крепкие комки однородной массы. Небольшое количество этих комков можно измельчить в фарфоровой ступке или размолоть в мельнице, а затем просеять через соответствующее сито, желательно более мелкое, например № 65. Если взять этой смеси 100 г и к ней добавить 28 г пороховой мякоти, хорошо перемешать, это и будет стопроцентный компонент, который нам заменит легкий металл.
_____ ПИРОТЕХНИК її III IIMMMIMHMMMHMiW (■imW'IIMII ЩЦІМЙШІ
От того, что мы хотим получить, можно путем добавления или уменьшения такой смеси варьировать скорость горения, количество дымообра-зования, яркости и других характеристик полученной смеси. Меньшее ее содержание в составе даст спокойное горение, и чем больше добавка из такой смеси, тем скорее будет проходить реакция, а значит, и горение состава. Сама же такая смесь очень активна, негигроскопична и оттого может долго храниться. По такому же методу можно приготовить и двухкомпонентную смесь, которая долго хранится и негигроскопична: нитрат калия — 50% и сера — 50%.
Хорошее пламя получается от смеси такого рецепта: нитрат стронция — 70%; нитрат калия — 7%; сера — 7%; уголь древесный — 6%.
Но это пламя розового цвета. Если его несколько обесцветить, дать ему добавку из алюминиевой пудры или антимония, можно получить яркое белое пламя; однако надо запомнить, что эти добавки сделают состав более чувствительным и не подлежащим долгому хранению. Дымный или черный порох, а также пороховая мякоть, обеспечивают довольно яркую всйышку. Порох можно взять и готовый, можно из него приготовить пороховую мякоть. Но пороховую мякоть для вспышек лучше приготовить самим, потому что в готовый порох добавляют некоторое количество клея при его гранулировании, а значит, такая мякоть будет гореть с меньшей скоростью, нежели пороховая мякоть, приготовленная самим пиротехником. Да и размолка сухого пороха дело опасное и трудоемкое. Конечно, безопасность важнее всего. Рецепт изготовления черного пороха всем знаком, но приготовляя пороховую мякоть вновь, — необходимо помнить, что составляющие химикаты должны быть размолоты до пылевидного состояния. Особо следует сказать о древесном угле, который надо брать только из лиственных легких пород древесины. Далее мы еще не раз будем говорить о смесях, образующих пламя, поговорим обязательно о технологии их изготовления, об инструменте, средствах защиты и оборудовании для их изготовления, хранения и перевозок.
Получение дымовых эффектов можно осуществить несколькими путями. Для этого надо знать, какого цвета дым мы хотим иметь. Иногда его приходится получать из материалов, которые не нуждаются в предварительной обработке. Так, получить белый дым можно сжиганием непригодной к употреблению соломы или травы, веток деревьев, положенных на предварительно разведенный костер. Черный дым можно получить от сжигания смолы хвойных деревьев, мазута или асфальта, сжигаемых на костре при большой температуре. При малой температуре эти материалы будут выделять белый дым. Отслужившие свой срок и непригодные к дальнейшему использованию автомобильные покрышки при горении дают черный дым, однако этот дым небольшой густоты. В населенных пунктах пользоваться такими дымопусками не рекомендуется из-за того, что прекратить на короткое время горение покрышек невозможно, а разгораются они очень долго, да и продолжают гореть, когда надобность в дымопуске уже отпала. Естественно, что такие очаги дымопусков передвинуть по кадру крайне трудно, а чаще просто невозможно. Лучше все эти дымовые эффекты получать за счет использования способности нефтепродуктов и других химикатов реагировать с компонентами атмосферного воздуха, чаще всего с его влагой. Такие реакции дают четыреххлористое олово (SnClJ, четыреххлористый кремний (SiCl4), четыреххлористый титан (ТіС14) и другие хлорсодержащие кислоты. Чем выше содержание хлора, тем большее будет дымообразование. Старые пиротехники нашего цеха хорошо помнят, как пользовались титаном четыреххлористым для образования «тумана» на болоте, «зимней метели» и «пурги». Пробовали использовать его и при создании искусственных облаков. Емкость с жидкостью выстреливалась из мортиры, при помощи замедлителя и разрывного порохового заряда в воздухе емкость разрушалась, титан четыреххлористый вступал в реакцию с атмосферным воздухом, образуя облако. Метод этот был трудоемким и весьма опасным.
Была попытка внедрить в производство создание искусственных облаков с помощью реакции четыреххлористого кремния с воздухом атмосферы. Это соединение еще более вредное, и от него отказались быстрее, чем от использования четыреххлористого титана. Потом изъяли и последний, после того, как емкость, вмещающая около 2 кг жидкости, взорвалась в руках пиротехника Б. Широкова. Он получил большое отравление, травмы слизистых оболочек органов дыхания, из-за'чего долгое время находился на лечении.
Белый дым, вернее, туман, можно получить за счет использования реакции между двумя веществами, химическое воздействие которых приводит к образованию мельчайших капель, взвешенных в воздухе. Экспериментально была опробована возможность получения дыма за счет реакции аммиака (NH3) и соляной кислоты (НС1). В результате этой реакции, образующийся аэрозольный хлорид аммония (NH4C1) превращается в большое облако хорошего белого, слегка подсиненного цвета. В реакцию вступают почти
все 100% химикатов. Однако надо помнить, что соляная кислота (НС1) вредна для здоровья человека. Такие эффекты допустимы только в пустыне, при этом надо постоянно следить за направлением ветра, чтоб не отравить съемочную группу. Примерно такой же эффект можно получить испарением или неполным сжиганием различных масел и других нефтепродуктов малого октанового числа: битума, мазута, асфальта. Этот метод используется в Советской армии в наземных дымозавесчиках — Т.Д.А. и в Военно-Морском флоте на специальных катерах. Этот метод используется и у нас при создании в павильонах так называемого «тяжелого дыма».
Эффекты легкого светлого тумана можно получать испарением сжиженных или замороженных до твердого состояния газов. Но это краткосрочный эффект, за исключением одного — испарения отвержденной, замороженной углекислоты в горячей воде, что нашло большое применение в последнее время даже на эстраде. Лучшим методом получения искусственных облаков и туманов до сего времени остается сжигание специально приготовленных пиротехнических смесей, которые содержат в своем составе или образуют в процессе реакции, во время горения, различные дымообразующие вещества. Рецептов изготовления таких смесей очень много, и у каждого — своя технология изготовления, свои меры предосторожности и техники безопасности. В дальнейшем мы рассмотрим многие составы белого дыма и цветных дымов, ознакомимся с .технологиями их изготовления в условиях пиротехнических мастерских
11,111^1 F.I.UJ і ИШ і W Ul 11 ,lh 11Щ m 11 і I № ИІИ 1'1 Ul 11В йіміимидмимим при киностудиях страны, условиями хранения, перевозки и безопасного использования на местах.
В пиротехнической литературе встречается рецепт создания белого дыма за счет сжигания белого фосфора, продукты горения которого реагируют с влагой воздуха и конденсируются. При этом образуется облако белого дыма, но с ним образуются сразу две очень вредные, ядовитые кислоты: мета-фосфорная и ортофосфорная. Надо помнить всегда, что фосфор (Р) токсичен, особенно белый, опасен при применении, да еще и образует кислоты. В пиротехнике он мало применим. В кинопиротехнике белый фосфор не применяется.
Если хорошо разогреть различные масла, но не дать им воспламениться, то при испарении будет образовываться туман за счет смеси с влагой воздуха. Есть такие установки в различных странах. По свидетельствам многих наших сотрудников — лучшие установки, среди бывших демократических кинопиротехников, имеются у немцев на киностудии «Дефа». У нас неплохие связи с ними, мы уже давно имеем чертежи данных установок, у нас даже есть одна такая разобранная установка, но она давно пылится в одной из мастерских. Так что данной действующей установки у нас нет. Правда, у нас есть установки, при помощи которых вырабатывается дым на основе разогретых паров трансформаторного масла; но они неудобны, неприглядны, тяжелы и громоздки. Для работы к ним необходим огромный баллон с углекислым газом для резкого охлаждения масляных паров, поэтому на натурных съемках они непригодны. Армейские же дымозавесчики на автомобилях и катерах, о
ПИРОТЕХНИК которых уже кратко упоминалось, покрывают дымом чересчур большие площади. Надо заметить, что масляный туман более устойчив, нежели при- ... меняемый нами в шашках НДШ, и рассеивается | в воздухе труднее. Его эффект лучше, чем при | сжигании шашек, но он намного дороже, поэтому | к нему в кино и редко прибегают.
Испарение масел можно осуществлять в струе раскаленных газов. Но такая установка пока еще дорога, хотя лабораторные, пробные работы на ней проводились. Эксперименты показали, что при таком способе можно получать не только белый дым, но и дымы любого цвета. В этом случае предварительно в масле надо растворить соответствующий жирорастворимый краситель, который легко возгоняется при сравнительно низких температурах. Получение белого дыма при киносъемках испарением сжиженных газов или замороженных газов — и экспериментально, и на съемках удавалось получить эффект «испарения» с помощью жидкого азота, разлитого по поверхности. Чтоб получить эффект тумана, надо раз- 4 ливать жидкий азот дорожками перпендикулярно к оси объектива съемочного аппарата. Жидкий азот будет вступать в реакцию с влагой воздуха и конденсировать ее вокруг молекул азота, охлаждая их до относительно низкой температу- £ ры. За счет разбрасывания кусочков замороженной углекислоты можно получить эффект тумана, в особенности после дождя и когда нет солнца. Погруженные в воду куски углекислоты имитируют ее кипение с выделением холодного пара — тумана.
Получить белый дым пиротехническим способом можно двумя путями или, скорее, видами. Эти два вида резко отличаются один от второго. Одни составы, смеси, содержат дымообразующие вещества уже в себе, в качестве компонента. Мы уже говорили, что такие смеси содержат окислитель и горючее. Теперь мы поговорим и о химика-те-дымообразователе. Нам знакомы многие дымообразующие химикаты, они чаще всего выступают и в качестве горючего. Это те химикаты-горючие, которые при своем горении выделяют еще и много газообразных продуктов. Среди них: антрацен, нафталин, хлористый аммоний, дициандиамид, гексахлорбензол, гексахлорэтан и другие. Эти вещества не требуют большой температуры при своем сгорании, и дым образуется за счет охлаждения частиц, не сгоревших, а возгоняемых и переходящих в твердое состояние. В белых дымах, в смесях для получения белого дыма чаще других применяют хлорид аммония (NH4C1), аммоний хлористый, нашатырь; его температура плавления около 30Q°C, а участвует в дымообразовании около 80% всего количества, которое находится в смеси. Аммоний хлористый лучше других соединений аммония пригоден в смесях по всем своим показателям, так как менее гигроскопичен, не токсичен и достаточно летуч, пригоден к испарению. В качестве дымообразователей применяются и различные масла, а также нафталин и антрацен.
Надо заметить, что эти химикаты, естественно, выполняют и функции горючего. В качестве окислителя с такими горючими, как правило, применяют хлорат калия (КС1О3) — бертолетову соль.
Самый старый рецепт белого дыма, полученный пиротехническим путем, то есть от смешения нескольких компонентов, известен в России под названием «Смесь Ершова». Военный пиротехник Ершов предложил его в качестве дымовой завесы, чтобы скрыть на море маневры кораблей от противника:
1. Хлорат калия — 20-30%;
2. Аммоний хлористый — 50%;
3. Нафталин — 20%;
4. Уголь древесный — 0-10%.
Внимательно читая этот рецепт, можно заметить много особенностей, на которые надо обратить внимание. Во-первых, нафталин, его присутствие в рецепте белого дыма. Мы привыкли, что нафталин при горении выделяет черное образование — сажу. Здесь же общее сочетание химикатов в смеси подчинило нафталин своему воздействию, и он выделяет белый дым, сгорая почти весь, то есть реакция идет дальше, чем при выделении черного дыма. Во-вторых: нам позволено бертолетовой соли брать от 20 до 30%, а древесного угля от 0 до 10%. Только за счет этой вольности и даже благодаря ей можно сделать несколько вариантов составов. Но не надо обольщаться, такая смесь и подобные ей обнаруживают отрицательный результат тем, что при горении дают неожиданные вспышки. Эти вспышки нельзя предусмотреть, и они появляются в самый неожиданный момент. В кинопиротехнике с такой смесью работать не рекомендуется — будет брак съемочного материала— «мигание*, особенно если дымопуск происходит близко от съемочного аппарата.
Да и при маневрах кораблей вспышки на катере-дымзавесчике демаскировали его самого, и он становился мишенью для пушек противника. Однако основа использования различных химикатов, их сочетание в смесях была сделана Ершовым. При дальнейших исследованиях и разработках «смеси Ершова» и ей подобных добавили химикаты-пламягасители, что сделало такие смеси уже без появления вспышек.
Лучшими пламягасителями показали себя углекислые соли: мел, сода, углекислый магний и другие. Эти соединения при своем сгорании легко выделяют углекислый газ — СО2; он-то и препятствует появлению вспышек, не дает нашим смесям гореть огнем. Все мы пользовались дымсоставом павильонным, многие из нас делали сами павильонный дым-состав и при этом вводили мел в качестве одного из компонентов этой смеси. С другой стороны, пламягасители это химикаты, останавливающие горение, препятствующие продолжению реакции, и вводить их в составы надо осторожно. В зависимости от общего соотношения всех химикатов в составе, от того эффекта, которого мы добиваемся, пламягасители можно вводить до 10-15% от всего количества смеси. Обычно его вводят от 3 до 7%. Его количество должен определить сам пиротехник на основании нескольких проб различного сочетания всех компонентов с пламягасителем или делать состав точно по готовому рецепту, разработанному и проверенному годами, как это происходит у нас в цехе. И даже в таких случаях после первой партии любого изделия надо проверить его горение и тот ли получается эффект, которого мы добивались.
Новая партия любого химиката должна проверяться в изделиях. Только путем проб и проверок можно составить рецепт смеси для дальнейшего изготовления пиротехнических средств. Только пиротехник, испробовавший химикат в смесях, может дать жить рецепту, неся полную ответственность за его безопасные и эффектные данные. Только на основе практических испытаний можно утверждать, что смесь, сделанная по данному рецепту и технологии, даст необходимый эффект. Где бы вы ни прочитали, где бы вы ни встретили рецепт пиротехнического изделия, как бы ни был высок авторитет ученого, рецепт без пробы нельзя принимать на веру, на слово. Его надо обязательно проверить практически, и если вас что-то не устраивает, то он, этот рецепт, может послужить основой той смеси, которую вы хотите сделать для своего эффекта. От него, от любого рецепта начинаются наши пробы, наши искания, испытания. Меняются химикаты, меняются даже стандарты химикатов, появляются новые вещества, и их надо проверять, испытывать. Надо всегда стремиться к тому, чтобы рецепт смеси, готовое пиротехническое изделие, сделанное вашими руками, отвечали всем вашим требованиям и полностью обеспечивали тот эффект, который был задуман и необходим. При этом никогда нельзя забывать о технике безопасности изготовления и применения нашей продукции, ее себестоимости.
Мы немного отвлеклись от темы белых дымов, но то, что было сказано немного ранее, на наш взгляд, применительно не только, к рецептам и изделиям белого дыма, но и ко всем пиротехническим изделиям.
Дымообразующие химикаты _______________
■■х*'.: 11 й і г< і । .■ 11 п пі»і мит тітіь~іммммігг imwhmmmmwhwwwwim л И । >ґ l wwm—*mwh
Однако вернемся к белым дымам, вернее рецептам белых дымов второго типа. Составы второго типа белых дымов изготавливают на основе металлохло-ридных соединений. Однако в пиротехнике они не могут быть использованы из-за своей токсичности и из-за того, что в таких смесях нужны углероды. Углероды в таких составах сгорают не полностью, и эти несгоревшие частицы углерода образуют сажу. А она, как известно, черная. Значит дым будет серым, вернее, не чисто белым. Вот примерный рецепт из множества подобных соединений: СС14 — 37%; Zn — 63%.
Четыреххлористый углерод (СС14) с цинком (Zn) горят хорошо, но выделяют хлорный цинк — ZnCl2, и углерод — С, который будет черным, a ZnCl2 — ядовитым дымом серого цвета. Поэтому все современные рецепты белого дыма, даже в армии, вместо металлохлоридных соединений основываются на использовании гексахлорбензола — С6С16 и гексахлоретане — С2С1е. Рецепты нашего цеха основаны на окислителе бертолетовой соли КС10д — хлорате калия и горючих: аммонии хлористом NH4C1 — он же и дымообразующий компонент, канифоли С2ОНЗОО и сыром буроугольном воске с небольшой добавкой мела СаСО3, выполняющего функцию пламягасителя и поглотителя свободного хлора в рецептах павильонного дымсостава.
Составов и смесей черного дыма на киностудиях страны существует очень много. Все они основаны на горючем, которое представляют нафталин и антрацен, и окислителем, которым, как правило, является хлорат калия или бертолетова соль. Наш ; цех полностью перешел на смесь из двух компонен- і тов: хлората калия (бертолетова соль) (КС1О3) — 55% и антрацена (С14Н10) — 45%. Долгое время 5 мы изготавливали смесь для шашек черного дыма, ; где основным горючим (более 40%) был нафталин и лишь 4% было антрацена. Как уже говорилось выше — нафталин сублимированный по цене выше антрацена, да и летучесть у него довольно высокая; значит химическая стойкость этих смесей была хуже, чем у теперешнего нашего рецепта. Черный дым при сгорании таких смесей получается и образуется за счет сажи из углеводородной группы горючих (нафталин CJ0H8, антрацен С14Н10) при их неполном сгорании в таких смесях. Сейчас в нашем цехе только в исключительных случаях, когда нет антрацена, используют в качестве горючего в смесях черного дыма нафталин. Несколько лет назад сложилась в цехе обстановка, когда на складах не оказалось шашек черного дыма, не оказалось и нормального антрацена, который обычно использовался для их изготовления. Но было большое количество антрацена, непригодного к использованию в таких смесях из-за его насыщенности различными маслами. Пиротехники (том числе и автор этой книги) за короткое время разработали новый рецепт і смеси черного дыма для шашек № 1 и вывели цех из очень трудного положения. Можно было бы перейти на старый рецепт, но нафталина на складах достаточного количества не оказалось. Надо было использовать антрацен. Вот состав этой смеси: бертолетова соль — 50%; нафталин сублимированный — 22%; антрацен технический — 23% .
Из-за плохого антрацена очень усложнилась технология изготовления смеси. Надо было сначала смешать пропущенный через вальцы антрацен и нафталин, т. е. соединить механически два горючих, лишь затем вводить хлорат калия и тщательно перемешивать. Такого состава очень много налипает на стенки смесителя, и это создает дополнительные неудобства в работе, да и смешивать такой состав надо более длительное время. По дымообразованию этот состав превзошел все виденные смеси, обычная шашка горит вдвое дольше по времени, образуя весьма густое и черное облако. Есть у такой смеси и другие положительные качества: состав весьма стоек к механическим воздействиям и потому безопасен и в производстве, и в хранении, и в перевозках. К недостаткам его надо отнести то, что при таком обильном содержании масел в составе, ими быстро пропитывается бумажная гильза и, конечно, длительному хранению он не подлежит. Шашки, напрессованные таким составом, должны быть использованы в течении одного года. Есть и другие рецепты смесей для получения черного дыма: гек-сахлорэтан — 60%; магния порошок №4 — 9%; нафталин (антрацен) — 21%.
Как видим, рецепт разработан на металлохлоридной основе, где окислителем является гексахлоретан, и горючих два — магний, порошок которого легко окисляется и хорошо горит, поддерживая высокую температуру при реакции, и дымообразующее горючее нафталин или антрацен. Эта смесь выделяет очень хорошее дымообразо-вание, но горит очень быстро и чувствительна к механическим воздействиям, а поэтому опасна не только в производстве, но и при пользовании та- | кого состава шашками. К тому же у гексахлор-этан а есть большой недостаток — летучесть. Однако при наличии этих химикатов и при недостатке других можно делать шашки черного дыма и по такому рецепту. Но есть и еще рецепты, где гек-сахлорэтан заменен гексахлорбензолом: гексахлорбензол — 60%; магний — МПФ-3,4 — 30%; нафталин — 10%.
Или такой: фторопласт (тефлон) — 55%; магний — МПФ-4,3 — 29%; антрацен — 16%.
Эти два рецепта были опробованы, и по ним ; получили хорошие смеси, выделяющие большое количество черного дыма. Но на производство таких смесей идут более дорогие химикаты, смеси получаются более чувствительными по сравнению со смесью хлорат калия плюс антрацен, да и дороже, ij. поэтому на практике они употребляются очень ред-ко, как крайний выход из положения. Попутно надо сказать о том, что при изготовлении смесей черного дыма, при работе с этими химикатами, особенно с антраценом, надо помнить, что они токсичны, могут вызывать аллергию и раздражение открытых
Разработка рецептов черных дымов
частей тела, что длительный контакт может привести и к другим, более опасным заболеваниям. Поэтому необходимы все меры предосторожности и обязательны средства защиты, которые предусмотрены технологией изготовления смесей и изделий черного дыма.
Методом химической реакции, то есть традиционным методом получения цветных огней или получения белого и черного дыма, пока еще не удалось добиться больших результатов при получении і дымов других цветов. Здесь успехи пиротехников невелики. Есть только один рецепт, заслуживающий внимания, рецепт смеси получения желто-оранже- 5 вого дыма: магний — МПФ-3 — 16%; гексахлорэ- j тан — 48%; оксид железа (Fe2O3) — 36%.
Окраску этому дыму дает хлорное железо (FeCI2), которое является летучим при повышенной темпе- , ратуре, при которой горит данная смесь. Соединяясь с кислородом воздуха и водой, находящейся в воздухе, охлаждаясь при температуре воздуха, продукты горения превращаются в облако дыма. Есть рецепты получения оранжевого дыма соединений нитроцеллюлозы с анилиновыми красителями, но в условиях нашего цеха и других пиротехнических < мастерских такое производство невозможно. Однако цветные фильмы, особенно фильмы-сказки, для своего производства потребовали и цветных дымов. Основные рецепты цветных дымов разработаны на технологии возгонки органических красителей. В таких смесях краситель за счет большой температуры других компонентов переходит в парообразное состояние, мельчайшие частицы воды с этим паром окрашивают химикат, который являет собой газообразующее, дымообразующее вещество. Вот примерная схема построения рецепта цветного дыма: органический краситель — 30-50%; углеводы (лактоза, сахар пищевой, дициандиомид) — 20—35%; хлорат калия — 22-33%; бикарбонат натрия (или калия) — 3-10%; керосин или парафиновое масло — 2-4%; инфузорная земля (SiO2) — 0-4%; оксид железа (Fe2O3) — 0-3%.
Попутно надо заметить, что в таких смесях, если убрать краситель того или иного цвета, основа смеси — окислитель, горючее и дымообразующее вещество — дала бы белый дым, с довольно большой интенсивностью горения. Вводом жирорастворимого органического красителя мы перекрашиваем белый дым в любой нужный нам цвет и понижаем скорость горения такой смеси. Зная это правило и схему построения рецепта, можно сделать или подобрать смесь любого цвета. Внимательно и с пристрастием осмотрев схему построения рецепта, мы не найдем здесь вредных или токсичных химикатов, однако меры безопасности, предусмотренные технологией изготовления шашек цветных дымов, надо соблюдать неукоснительно, да и жирорастворимые красители с тела человека отмываются очень трудно. Эффекты, создаваемые комбинациями различных дымов бывают очень впечатляющими. Так, из сочетания белых, черных и оранжевых дымов удавалось создать эффекты пожаров больших городов, не употребляя ни одного очага пламени; особенно сильны такие эффекты на общих планах. Когда же постановочная группа переходит к съемкам средних и крупных планов пожара, конечно, здесь не обойтись без огня, без очагов огня, и опять мы будем прибегать к помощи цветных дымов: черному и красному, а белый дым выделяется при горении декораций, и его, как правило, хватает. Стоит просмотреть заявки кинокартин на пиротехнические материалы для батальных фильмов, мы увидим, что наибольшее количество после белых, которые требуются к лирическим фильмам, занимают черный и оранжевый дымы. При производстве фильмов по сказочным сюжетам требуются дымы самых разных цветов и оттенков. Нам самим приходилось делать шашки различного цвета дымов и использовать их, подчас не зная, для чего их применяют в тех или иных кадрах. При просмотре фильмов не всегда удается увидеть эти кадры, потому что дымы ие всегда правильно снимаются оператором, и в картину привносят лишь диссонанс, и кадры, снятые с дымами, выбрасываются из картины или переснимаются заново.
Газообразующие пиротехнические смеси Требования, предъявляемые к таким смесям.
Некоторые рецепты таких смесей
В кинопиротехнике зачастую возникает необходимость получения «эффекта длительного дымопуска». Как правило, это связано с макетами больших заводов, химических комбинатов, металлургических и коксохимических производств. Каждый понимает, что взрывать и поджигать данные объекты «в натуре» или даже декорации в натуральную величину — чересчур дорогое удовольствие (к примеру, город Мост в Чехословакии — один на весь мир, да и тот уже разрушен). Если вспомнить фильм по роману А. Толстого «Гиперболоид инженера Гарина» и разрушающийся химический комбинат, взрывающиеся цистерны с газом, химикатами и нефтепродуктами, то можно себе представить стоимость всего этого, если бы все это было «в натуре». С другой стороны, без этих кадров было бы трудно представить огромную разрушающую силу нового изобретения гениального маньяка. Был сделан макет огромного, грандиозного предприятия, и чтобы оживить его, показать работающим — были применены все средства воздействия на зрителя. Главными, конечно, были пиротехнические эффекты. Сначала это были дымы, в основном цветные, и несколько вспышек, имитирующих работу сварщиков и поток раскаленного металла. Цель была достигнута. Было видно, что предприятие работает, живет, хотя на общих планах не было ни одного человека. Появился бы человек, и все было бы нарушено. Зритель бы понял, что ему показывают макет. Путем монтажа нам показали несколько кадров в декорациях, а потом, в дальнейшем, началась катастрофа, где пиротехники применили все-средства для ее осуществления. О жирорастворимых красителях уже мы говорили, в этом фильме применялось несколько видов таких красителей. Плюс, оператор использовал в своей работе фильтры различных цветов. И, заодно, применялись газообразующие пиротехнические смеси.
Как правило, в пиротехнике для киносъемок состав газа не имеет значения. Главное к нему требование — нетоксичность. Однако при разработке смесей, при составлении рецептов необходимо учитывать особенности каждого химиката-компонента — поставщика газа. Наибольший газовый объем на одну грамм-молекулу реагирующих компонентов смеси можно достичь, получая в продуктах горения газы с малым молекулярным весом. Так, выяснили, что в объеме 22,4 литра различных газов будет: водорода (Н) -2 г; водяного пара, который при расчетах рецептов считается газом (Н20), — 18 г; азота (N) — 14 г; окиси углерода (СО) — 28 г; кислорода (О) — 32 г; углекислого газа (СО2) — 44 г.
Стоит обратить особое внимание на вес каждого газа в одинаковом объеме, потому что сгорание химиката с выделением различных газов будет нашей целью при изготовлении пиротехнических специальных изделий.
Итак, мы видим, что лучшим показателем в этом ряду будет вес водорода — 2 грамма, худшим — у углекислого газа, двуокиси углерода (СО2) (данный газ нам не нужен не только потому, что он тяжелый, но, и потому, что водород является продуктом горения лишь в редких смесях, следовательно, дабы получить его 22,4 литра надо сжечь много химикатов). Несмотря на неблагоприятное соотношение веса и объема углекислого газа = 44 грамма в 22,4 литра, образования этого газа редко удается избежать. Водяные пары — 18 граммов — тоже нужно считать газом при расчете газообразования. Стоит обратить особое внимание на азот (N), хотя известно, что азот является инертным газом, да и в объеме 22,4 литра его будет 14 граммов. Пиротехники из этого сделали вывод, что при расчете рецепта в качестве окислителей надо брать нитраты, так как именно в нитратах содержится газ азот и он выделяется при сжигании. Наиболее приемлемым нитратом является нитрат аммония (NH4NO3) — он не токсичен, температура плавления самая низкая из всех известных нитратов, очень низкая и скорость горения. Однако у нитрата аммония есть и недостатки — гигроскопичность, слеживание, перекристаллизация. Есть, конечно, и другие нитраты, но они по разным причинам менее пригодны для наших целей. Одни по своим химическим и особенно физическим качествам, другие слишком дороги, третьи — выделяют много вредных ядовитых веществ и применяться не могут. В качестве катализаторов в таких смесях чаще других использовали бы бихроматы калия (К2Сг2О4) и аммония ((NH4)2Cr2O7), но эти химикаты крайне ядовиты, и их вы не встретите в наших рецептах. Самым безопасным катализатором у пиротехников по праву считается * ми л ори», или железосинеродистое железо (Fe4[Fe(CN)J3). Этот химикат нам знаком, он встретится нам и в дальнейших рецептах некоторых пиротехнических изделий, мы о нем говорили, когда знакомились с химикатами, наиболее часто встречающимися в пиротехническом производстве. Вот пример рецепта газообразующего состава: нитрат аммония (NH4NO8) — 79%; «Милори» (берлинская лазурь) (FeJFe(CN)e]g) — 9%; уголь древесный (С) — 12%.
Эта смесь при своем сгорании дает чистый азот. Существуют большие промышленные установки — гиганты для получения азота на нужды химической промышленности и сельского хозяйства. При помощи пиротехнического состава можно получить чистый кислород в газообразном состоянии. Советский ученый, академик Капица, будучи в ссылке, разработал наиболее дешевый способ для получения газообразного кислорода в промышленных установках. Лабораторию он организовал в сарае и, несмотря на ссылку, занимался любимым делом. В результате страна получила самые мощные и самые рентабельные в мире промышленные установки по получению газообразного чистого кислорода. Рецепт получения чистого газообразного кислорода пиротехническим путем такой: нитрат натрия — 74-80%; железо (порошок) — 10%; окись бария (ВаО2) — 4%; стекловолокно -- 6-12%.
Эта смесь дает 34% кислорода в весовых частях от 100% сжигаемой смеси. Это очень большой процент выхода чистого кислорода. В литературе по пиротехнике и по химии встречаются и другие рецепты получения чистого газа пиротехническим путем, и человеку, интересующемуся этой стороной, всегда можно найти не только рецепт, но и описание технологического процесса. Есть и другие смеси, при помощи которых можно получать чистые газы таким путем, но эти смеси очень плохо загораются; они требуют для воспламенения сильного начального импульса. Иногда для воспламенения таких смесей, где температура горения очень высока, изготавливают два состава: воспламенительный и переходной. Внимательно читая указанные рецепты, мы заметим, что в них нет компонентов с малой температурой горения. Вот рецепт воспламенительного состава для указанных газообразующих смесей: NaC108 — 60%; Fe — 20%; ВаО2 — 10%; стекловолокно — 10%.
Смесь по такому рецепту изготавливают и прессуют в виде звездки отдельно от изделия, и лишь затем эту звездку впрессовывают в изделие перед непосредственным зажиганием. Есть и другие виды нанесения воспламенительных смесей, также много других воспламенительных составов, которые предназначены для различных пиротехнических изделий.
Воспламенительные составы, изделия и их элементы.
Назначение воспламенительных составов в пиротехнике и требования, предъявляемые к ним
Вы уже знаете, что существуют составы пиротехнических изделий, весьма инертных к небольшим или непродолжительным источникам воспламенения. Например, их нельзя зажечь электровоспламенителем или обычной спичкой, а некоторые не загораются от специальной спички (запала) или небольшого отрезка стопина. В предыдущей главе мы ознакомились с некоторыми рецептами газообразующих смесей и пришли к выводу, что таким смесям необходим специальный воспламенительный состав, который передал бы необходимую температуру данным изделиям по нашей команде. От простой спички не загорится дымовая шашка заводского изготовления, твердое ракетное топливо и т.д. Есть много различных пиротехнических изделий, которые загорятся только от мощной ветровой спички, отрезка стопиновой нити, или имеют воспламенительный, а иногда и переходный составы в одном изделии.
Требования к воспламенительным составам заключаются в том, чтоб они, эти составы, прогрели определенный участок основного состава до температуры, необходимой для вызова горения этих основных составов, чтобы реакция между компонентами основного изделия началась. Мы уже знаем, что чем вы-ше температура горения основного состава, тем хуже он загорается и тем сильнее по температуре должен быть воспламенительный состав. Воспламенительные составы должны отвечать требованиям, предъявляемым к данным составам. Вот эти требования:
— легко воспламеняться от сравнительно небольшого импульса (электровоспламенитель, ветровая спичка, небольшой отрезок стопиновой нити);
— температура вспышки любого из таких составов не должна превышать 500°С;
— иметь температуру горения намного (200—500°С) выше, чем те составы, которые мы поджигаем;
— в процессе горения образовывать большое количество жидких шлаков, которые остаются после сгорания на поверхности поджигаемого состава.
Шлаки, упомянутые выше, находясь в состоянии разогрева при высокой температуре, увеличивают время прогревания состава, который мы поджигаем. Чтобы продлить время горения воспламенительных составов, их, как правило, прессуют. Однако есть и другие виды передачи температуры — простая добавка сверху или в месте поджигания в виде пасты, которая потом подсохнет и образует одно целое с основным составом. У нас в цехе есть такие изделия, которые требуют воспламенительный состав; самые распространенные из них — малые пиротехнические шашки белого дыма № 5 и № 6 и черного дыма № 3. Если аккуратно расколоть звездку сигнального патрона сверху вниз — можно легко проследить, что она сделана из трех составов. Большая ее часть будет состоять из основного состава, а малая часть из переходного и воспламенительного составов, где ясно просматриваются вкрапления дымного пороха. Воспламенительным составом в фигурных свечах является пороховая подмазка с введенным в нее клеем и разведенная на спирте.
При составлении рецептов воспламенительных составов должны быть использованы окислители, легко отдающие кислород при небольшой температуре горения. Такие окислители мы хорошо знаем: это хлораты, нитраты, перманганаты щелочных металлов. В качестве горючего здесь применяются химикаты, которые легко входят в реакцию с окислителями: это уголь древесный, идитол, антимоний, сера и другие химикаты. Из данного перечня химикатов становится понятно, что рецепты воспламенительных смесей близки по рецептуре к дымному пороху. В некоторых изделиях, как мы наблюдали на примере со звездкой сигнального патрона, именно дымный порох является воспламенительным составом. Если в основном составе содержится алюминий, как основное горючее, то в воспламенительном составе должно быть не менее 15—20% магниевого порошка. Такой воспламенительный состав обладает хорошими химическими и физическими качествами и может применяться в различных изделиях. Из теории мы знаем, что предпочтение отдается, как горючим, цирконию и титану: цирконий способен вступить в реакцию даже с окисью железа. Но смеси с этими металлами весьма чувствительны к физическим воздействиям — следовательно, в кинопиротехнике они не применяются. В кинопиротехнике, в таких составах, чаще используют в качестве горючего соединения кремния, марганца, свинцовый сурик (один или в комбинации с красной окисью (FeO2)). Такие составы считаются наименее опасными и не столь чувствительными. В ракетной и космической технике применяют составы с титаном и цирконием. Ведь
там нужна большая точность, более высокотехнологичное производство, аппаратура и оборудование — последнее слово техники в этой области, а также отличная организация техники безопасности. В условиях наших примитивных кустарных мастерских и с уровнем наших технических и технологических возможностей эти металлы неприемлемы. z
При производстве дымовых шашек мы напрессовываем воспламенительные и переходные составы на основной, так как эта технология нам подходит и по требованиям, и по оборудованию. В других случаях воспламенительные составы делают в виде пасты и такими наносят на изделие. При высыхании эти пасты становятся чувствительны к огню. Данные составы делаются или на спиртовом лаке, или на цементаторе со спиртом. Бывают пиротехнические составы или изделия из таких составов, которые плохо загораются даже от воспламенительного состава. В таких случаях пиротехники пользуются переходными составами. Переходные составы представляют собой комбинацию из двух составов: воспламенительного и основного. Переходный состав загорается от воспламенительного и, сгорая, поджигает основной состав. Комбинации переходного состава могут быть различными. Наиболее часто встречаются и употребляются смеси из двух составов: 50% воспламенительного и 50% основного; тщательно перемешанные, они насыпаются, напрессовываются на основной, на них насыпается воспламенительный и в таком порядке запрессовывается полностью изделие. Вот несколько рецептов воспламенительных составов:
I.
1. Нитрат калия — 75%;
2. Древесный уголь — 15%;
•3. Идитол ~ 10%.
П.
1. Нитрат калия — 75%;
2. Магний (порошок № 3 или № 4) — 15%;
3. Идитол — 10% .
III.
1. Нитрат бария — 48%;
2. Перекись бария — 30%;
3. Магний (порошок № 3 или № 4) — 13%;
4. Идитол — 9%.
IV.
1. Цирконий (порошок) — 65%;
2. Окись железа — 25%;
3. Окись кремния (SiO3) — 10%.
V.
1. Титан порошок — 25%;
2. Кремний — 25%;
3. Окись железа — 25%;
4. Свинцовый сурик — 25%.
VI.
1. Титан порошок — 32,5%;
2. Окись железа — 50%;
3. Цирконий (порошок) — 17,5%.
1. Титан порошок — 20%;
2. Кремний — 10%;
3. Цирконий (порошок) — 70%.
Последние четыре рецепта содержат в себе редкие на наших складах химикаты, и не всегда мы сможем воспользоваться ими, да и как говорилось
Воспламенительные составы
•WS1 //Z ЦІЛІ,і Г Ґі П111 HMWtff A4JJMIUW,iTi,1 ft ІЇЛЛШМіГЖПіМГУ P* 1H H fffl ЦИКЛ UW WA'I ft 11 ffl < MlWIO
выше — эти рецепты очень чувствительны, а потому опасны. Но знать данные рецепты вы должны. Также, как должны знать и, то, что эти смеси очень опасны при изготовлении, и запрессовывать их следует в растворе камфары в ацетоне.
Воспламенительные элементы служат для того, чтоб передать импульс огня к изделиям или их элементам с определенной скоростью. Такими элементами могут быть: нить стопина, пороховые добавки различной скорости горения, огнепроводный шнур, и другие зажигательные препараты и приспособления. Самым важным элементом в этих изделиях является паста на основе пороховой мякоти. После высыхания на изделии она должна легко загораться и передавать температуру изделию. К изготовлению стопина или стопиновой нити и приготовлению пасты из пороховой мякоти мы еще вернемся, но есть и другие варианты изготовления такой пасты. Вот пример:
1. Пороховой мякоти — 1 кг;
2. Декстрина — 30 г;
3. Подогретой воды — 50-100 г;
4. Спирта — 50-100 г.
Декстрин разводится в подогретой до 50-60°С воде, смешивается с пороховой мякотью и разбавляется спиртом до необходимой густоты или суспензии. В качестве воспламенителей может использоваться бумага, промазанная с двух сторон пороховой пастой и просушенная, фитили различной скорости горения. Хорошие фитили получаются при использовании такой технологии: растворить в десяти частях воды одну часть нитрата калия, селитры (KNO3). Хлопчатобумажный шнур замочить в этом растворе
ПИРОТЕХНИК llhWi1WWMi№MWirrf
на 6-8 часов. Вынуть из раствора и просушить, не отжимая. Более медленно будет гореть тот же шнур, если его пропитать в таком составе: нитрат свинца — 1 часть; вода подогретая — 10 частей.
Для поджигания фейерверочных фигур пиротехники часто пользуются зажигательными свечами, которые состоят из нитрата калия — 30%; серы — 10%; пороховой мякоти — 10%; воска (вара, пека) — 5%.
Хорошо перемешанный этот состав набивают в гильзу длиной 50 см и диаметром в 1 см. Заготовлен- і ные заранее гильзы предварительно пропитывают в растворе нитрата калия (1:10) для того, чтобы гильзы сгорали вместе с составом, постоянно обнажая пламя собственного состава. При изготовлении таких свечей состав насыпают не более пяти сантиметров и запрессовывают набойником с молотком. Можно внизу сделать деревянную рукоятку, можно нижнюю часть гильзы набить не горючим составом. Тогда такой свечой можно безопасно пользоваться. О мерах безопасности при работе с воспламенительными составами надо еще сказать, что, как правило, такие составы изготавливают малыми партиями. Там, где такие составы делаются в полужидком состоянии, — они не опасны. Но при этом надо строго следить, чтоб они не подсохли, и поддерживать их в таком состоянии. Подсохшие составы на пороховой мякоти не соскребать с посуды, а долить воды, и таким способом или размягчить, или растворить. Воспламенительные составы с порошками циркония и титана делаются не более 2-3 десятков граммов за защитным щитком, в очках, нарукавниках и прорезиненном или кожаном фартуке. Когда же эти составы выделяют газы (запрессовка в растворе камфары с ацетоном), необ-ходимо пользоваться противогазом. Работа с воспламенительными составами требует строгой пожарной безопасности, поэтому прежде чем приступить к их изготовлению, надо вынести из рабочего помещения все предметы, не имеющие отношения к данной работе. После работы все инструменты и приспособления, а также полы в помещениях должны промываться водой.
Замедлители и их назначение Некоторые рецепты замедлителей, изготавливаемых промышленностью, и возможности их изготовления в мастерских
Замедлители — изделия, которые необходи- , мы в пиротехнике почти так же, как и воспла- £ менители. Если нам надо взорвать какое-то пи- £ ротехническое изделие в воздухе или на определенном расстоянии над землей, или произвести взрыв над водой — мы пользуемся изделием, которое позволяет произвести взрыв после выстрела. Так сделаны военные электровзрывпакеты (ЭВП), так делаются многие пиротехнические изделия, например, «люсткугели», факелы на парашютах, имитаторы облаков воздушного пользования и другая продукция. В старину также пользовались замедлителями. Эту роль выполняла обыкновенная восковая свеча. У основания свечи насыпали порох, а когда свеча, догорая, поджигала его, порох взрывался и разрушал стены крепостей и других фортифи- * кационных сооружений. В наше время оборонные заводы изготавливают и поставляют нам заводские стандартные замедлители, рассчитан-ные на определенное время: от 0,5 до 3 секунд, | Пиротехнические изделия, снаряженные такими замедлителями, «срабатывают» точно в пристрелянном месте, что порой бывает немаловажным фактором при киносъемках. Там же, где не требуется такой точности, хорошими замедлителями зарекомендовали себя обрезки огнепроводного шнура.
Замедлители ___
It- - ■ ■ ■■■-■-ll.l.TNWIIMJfni» Гі.І'Мя'ДІІІІММіМИЯІИі ІІІ ІПІ Т І'У ІІ1І ІІ1Ї ІІ lll |JWWH«lWWM^»MHWW*>WW***M<»*OMMMfHaHrnimTTrTnr i"~M«MM*TTTirTr“~r~~~~~"TltMTTTT
Известно, что огнепроводный шнур горит со скоростью 1 см в секунду. Если учесть, что часть пороха высыпается из шнура во время различных манипуляций с изделием, то на одну секунду замедления надо резать шнур (отрезок) длинной 1,5 см. Если же у нас будет рассчитанное время на 1,5 секунды, надо резать шнур длиной 2 см, и т.д. Шнур режут острым ножом под прямым углом к его поперечному сечению. Никакие другие углы непригодны, так как произойдет высыпание пороха. Скорость горения заводских замедлителей примерно — 0,04 0,06 см/сек. В этих замедлителях используются в качестве горючих металлы: цирконий, титан, марганец, железо, никель; неметаллы — кремний и бор. Для увеличения скорости горения окислителями в этих изделиях служат хромат бария, хромат свинца и перхлорат калия. Вот некоторые рецепты замедлителей:
I II
1. Аморфный бор — 5%; — 10%;
2. Хромат бария — 95%; — 90%.
III.
1. Марганец — 44%;
2. Хромат бария — 8%;
3. Хромат свинца — 53%.
IV.
1. Марганец — 37%;
2. Хромат бария — 20%;
3. Хромат свинца — 43%.
V.
1. Марганец — 33%;
2. Хромат бария — 20%;
3. Хромат свинца — 36%.
VI.
1. Пераманганат калия — 56%;
2. Сурьма (металлический порошок) — 44%.
Некоторые рецепты в наших условиях, а главное, из-за наличия химикатов, реализовать просто невозможно. Правда, изготовление замедлителей не очень и нужно, так как можно пользоваться заводскими, с одной стороны, и, как уже было сказано в главе о воспламенительных составах, химикаты, входящие в составы замедлителей, являются токсичными, и смесь их опасна в обращении.
Надо отметить и тот факт, что замедлители сами являются весьма чувствительными к механическим воздействиям. Был случай, когда во время закрутки другой стороны «люсткугеля» произошел взрыв одного из них. Это явилось нарушением мер безопасности по обращению с такими чувствительными изделиями, которыми являются замедлители. Стоит посмотреть на список химикатов в рецептах, чтобы понять, что с замедлителями надо обращаться весьма осторожно. При их монтаже нельзя нажимать, ударять и тереть ту часть, где проступает состав. Нельзя монтировать замедлители и в готовое изделие. Они монтируются в пустые гильзы, предназначенные для каких-то изделий, требующих при своей дальнейшей технологии использование замедлителей.
Чувствительность
Химическая и физическая стойкость пиротехнических составов
В дальнейшем мы ознакомимся с технологией изготовления многих пиротехнических изделий. Заодно мы будем изучать совместимость тех или иных химикатов. И хотя мы уже многое знаем о свойствах и характеристиках многих материалов, мы должны знать о них еще больше. Дополнительная информация, дополнительные знания о материалах, с которыми приходится работать постоянно, еще никому не вредили. Важность этой информации надо учитывать для обеспечения безопасности при изготовлении, хранении, транспортировке и использовании пиротехнических изделий. Надо твердо помнить о факторах, которые способствуют формированию опасных свойств пиротехнических составов, смесей, и по возможности их исключать. Вот некоторые из данных факторов:
1. Высокая чувствительность смесей хлората калия с фосфором.
2. Чувствительность к удару и трению всех хлоратов в смесях со следующими элементами и веществами: серой, селеном, металлическим мышьяком, сульфидами фосфора, сульфидами мышьяка, сульфидами сурьмы, магнием, алюминием, цирконием, висмутом, титаном.
3. Особенно высокая чувствительность к механическим воздействиям смесей хлоратов с роданистыми, железными и железосинеродистыми соединениями.
4, Чувствительность к трению и опасность в обращении двойных смесей нитратов с магнием, алюминием, фосфором.
5. Высокая чувствительность смесей, окислителями которых являются: перхлорат аммония, перхлораты щелочных металлов, некоторые кислородные соединения свинца, особенно РЬО2.
6. Чувствительность пиротехнических составов ко всем видам воздействия с повышением начальной температуры. Это необходимо учитывать при просушивании составов пиротехнических изделий.
7. Значительно повышают чувствительность пиротехнических составов к механическим воздействиям и делают их опасными в обращении примеси песка, битого стекла и других твердых веществ. Поэтому в рабочих помещениях, на рабочих местах всегда должна быть чистота, лишние предметы и материалы, ненужные для данного изделия, а иногда для определенной операции, необходимо убирать.
Надо помнить и о том, что снижают чувствительность пиротехнических составов ко всем воздействиям добавки флегматизаторов, там, где есть возможность пользоваться этими добавками. Весьма взрывоопасны взвеси в воздухе таких материалов: угольная пыль, сера, сахар, лактоза, крахмал, декстрин, мучная пыль, алюминиевая пудра. В качестве причины может быть даже образование электрической искры в результате статического электричества. Йто электричество накапливается на оборудовании, и его периодически надо снимать. Это электричество может накапливаться и на одежде пиротехника, особенно если одежда сделана из синтетических материалов. Поэтому пиротехники для работы с такими материалами допускаются только в хлопчатобумажных костюмах и нарукавниках. При организации работ надо обязательно учитывать данные обстоятельства. Надо помнить, что у неспрес-сованных составов возможность возгорания или взрывания намного выше, чем у брикетированных. При работе с чувствительными смесями в помещении не должно быть рабочих, не занятых непосредственным процессом изготовления смесей. Как правило, с такими смесями работает один человек, максимум двое. Нельзя увлажнять двойные смеси нитратов и хлоратов с горючими металлами, так как коррозия металлов приводит к их уничтожению; металлы окисляются и пропадают. Нет смысла делать для длительного хранения такие смеси и с гигроскопичными солями. Такие смеси химически нестойки. Химически нестойки и смеси серы с магнием, но нитраты с серой и алюминием или магнием могут храниться более длительное время. Надо запомнить, что смеси, содержащие в качестве компонентов порошок магния и одновременно алюминия, чувствительны к воздействию влаги. В то же время порошок сплава алюминия с магнием (ПАМ) более устойчив против воды, щелочных и кислых воздействий. В смеси нитрат бария плюс алюминий может начаться реакция, если присутствует влага. При этом начнет образовываться аммиак (NH4), и можно почувствовать его запах. В таких случаях надо немедленно прекратить работу и вынести состав из помещения. Значит, в этой смеси присутствует влага, и нужно срочно выяснить, какой из компонентов содержит влаги больше допустимой нормы, и принять меры к ее удалению, к просушиванию химиката. Чаще всего влага бывает в нитрате бария. Надо помнить, что смеси нитратов с тяжелыми металлами, их соединениями (Pb(NOa)2; Cu(NO3)2), с магнием при увлажнении становятся химически нестойкими из-за прохождения обменной реакции. Смеси же этих и других соединений тяжелых металлов с алюминием химически более стойки. Алюминий быстрее покрывается оксидной пленкой, потому что данная пленка у него прочнее, чем, к примеру, у магния, и с ее помощью он защищает себя от коррозии. Смеси хлоратов с магнием химически нестойки и не рекомендованы не только к длительному хранению, но и к изготовлению. Не рекомендованы к применению смеси перекиси бария (ВаО2) с порошками алюминия. При попадании влаги в такую смесь температура ее может подняться до 100°С и алюминий превратится в инертное вещество. Нежелательны в составах, содержащих порошок магния, добавки солей аммония (NHJ; такие смеси будут гигроскопичны и в результате присутствия влаги (Н20) в этих смесях проявляется гидролиз и протекает кислая реакция (NH4C1 + Н2О = НС1 + NH4OH). В такой кислой среде интенсивно протекает коррозия магния, так как у него оксидная пленка более рыхлая, пористая, чем у алюминия. Порошок алюминия в таких смесях более устойчив. Коррозия порошков алюминия ускоряется, если в смеси есть порошки или соли меди и ртуть. Поэтому в одной смеси эти химикаты (Си + Al; Hg + Al) не допускаются. Составы, содержащие порошки железа, в большинстве своем химически нестойки.
Чувствительность
ііо yiWiW - r iii n fon tmr№mv<K iw^wri-i whwmwiiiht tur.rr і w.v лл .v. w Цв#ом*иж»<«Г>г» waotriwtf ьуьчїіу wrm w, iurr іїям»
Для улучшения качества и защиты порошка железа его «воронят», кипятят в масле. Мы часто говорим, что недопустимо вводить в хлоратные составы аммиачную селитру, потому что происходит обменная реакция, в результате которой (KC1OS + NH4C1 = КС1 4-NH4C1O3) появляется хлорат аммония (NH4C103) — вещество нестойкое, оно может привести к самовозгоранию и даже к самовзрыванию смеси.
Нельзя пользоваться инструментом, ситами одновременно и для хлоратов, и для нитратов. А такие, как КС103 и KNO3, — вообще несовместимы и способны возгораться даже при малом присутствии одного в другом. На протяжении многих лет бертолетова соль обрабатывается и смешивается в нашем цехе в кабинах с первой по пятую, а селитра — с восьмой по одиннадцатую. Может быть, что только благодаря такому строгому, жесткому разграничению, мы не имели самовозгорания в производственных помещениях цеха. Такие меры предосторожности должны поддерживать все последующие поколения пиротехников. Нельзя мешать хлораты с серой. Смеси такие химически нестойки, они могут загореться во время изготовления, прямо на столе под руками пиротехника. Смесь глицерина с перманганатом калия (КМпО3) самовозгорается через 10-20 секунд после смешения компонентов. Значит, их нельзя смешивать, кроме тех эффектов, которые необходимы при съемке. В таких случаях пользуются несколькими «считанными» граммами.
Все мы отлично понимаем, что все правила, все случаи перечислить невозможно, потому что появляются новые химические материалы, и. мы будем вводить их в свои рецепты, в свои смеси, но
________________________ПИРОТЕХНИК при обязательном соблюдении самых элементарных правил безопасности, которые требуют:
1. Изготовление экспериментальных составов в минимальных количествах.
2. При работе с новыми или незнакомыми материалами и рецептами обязательно пользоваться защитным щитком, очками, нарукавниками, перчатками, фартуком.
3. После изготовления состава пиротехник обязан проверить, хотя бы примитивным способом, этот состав на чувствительность к удару, трению, лучу огня; проверить его замачиванием, увлажнением малого количества состава, с последующим наблюдением за ним, а в дальнейшем и сжиганием.
4. При нагреве смеси, появлении необычного запаха пиротехник должен прекратить работу. Необходимо принять решение об отказе от дальнейшего использования этого рецепта, а готовая смесь должна быть уничтожена путем замачивания в воде и удаления растворимых химикатов. Рецептура смесей и составов лишь тогда допускается к серийному производству, когда состав испытан по всем возможным параметрам. Новые рецепты изделий и смесей должны быть теоретически обоснованы и практически подтверждены для дальнейшего ис
пользования.
Классификация пиротехнических средств, применяемых на фейерверках и при киносъемках
Все пиротехнические средства, применяемые при киносъемках и на фейерверках (и те, о которых мы уже говорили, и те, о которых речь пойдет ниже), — по характеру их действия, по создаваемому ими эффекту и специфике изготовления условно можно разделить на пять групп:
I группа — дымовые пиротехнические средства;
П группа — осветительные и сигнальные средства;
III группа — имитационные пиротехнические средства;
IV группа — фейерверочные пиротехнические средства;
V группа — вспомогательные средства и материалы.
Все эти средства, промышленного изготовления или пиротехнические изделия и эффекты, разработаны и проверены на практике в пиротехническом цехе киностудии «Мосфильм». Исключение составляют несколько рецептов, известных по различным литературным источникам от Цытовича до Шидловского и зарубежной периодической литературы, в основном переводных журнальных статей.
Дымовые пиротехнические средства при КИ- ji носъемках и дневных фейерверках находят самое широкое применение. Дымовые эффекты использу- J ются не только в батальных, но и во многих лирических кинокартинах, где создают эффект природных явлений: облака, туман. Находят дымы применение и в кинокартинах, где необходимо показать сельскую жизнь — дым из труб печей, костры, горение леса, хлеба; и городские пейзажи, которые нельзя себе пред- $ ставить без огромных заводов, фабрик, комбинатов с их постоянно дымящими трубами, иногда даже с цветными дымами. Правда, сейчас стало немодным показывать обилие дымов в кинофильмах, но от истории не уйти. Считалось, что чем гуще и выше дым — тем больше продукции дает предприятие. Дымовые эффекты необходимы при съемках фильмов сказочной и научно-фантастической темы. К числу пиротехни- $ ческих средств, обеспечивающих вышеперечисленные эффекты, относятся:
пиротехнические дымовые средства, изготовление которых организовано в пиротехнических ма- t стерских киностудий: ■<
— дымовые шашки черного дыма № 1;
— дымовые шашки цветных дымов различного цвета; ,Е
— малые пиротехнические шашки черного и ’■ белого цветов, называемые «МППЬ и различающиеся по номерам (3, 4, 5 и 6);
— дымовой состав белого дыма, пригодный для использования в условиях павильонных съемок и съемок в интерьерах других зданий;
Дымовые пиротехнические средства
— быстрогорящие дымовые составы — «дымовые вспышки» — черного, белого и многих цветных дымов.
Дымовые промышленные средства:
— шашки белого дыма — НДШ и ДМ-11;
— большие дымовые шашки — БДШ;
— ручные дымовые гранаты белого и черного дыма;
— генераторные установки, смонтированные на средствах передвижения;
— другие средства, выделяющие в основном белые и черные дыма.
Осветительные пиротехнические средства применяются для создания Цветовых эффектов, при съемках пожаров, для создания эффекта освещения боевыми осветительными средствами объектов и людей, при съемке батальных сцен, для имитации освещения фарами автомашин, блеска молний, отсвета костра и для многих других работ. К этой группе относится сравнительно небольшая группа сигнальных средств, применяемых для подачи сигналов при киносъемках и имитации действия сигнальных средств в боевой обстановке. К числу пиротехнических средств, обеспечивающих перечисленные эффекты, относятся:
1. Осветительные и сигнальные средства, изготовление которых организовано в пиротехнических мастерских киностудий: факелы белого и оранжево-красного огней, фальшфейеры белого и красного, желтого и зеленого огня, ручные парафиновые факелы, фотовспышки, парашютные осветительные факелы.
2. Осветительные и сигнальные пиротехнические средства промышленного изготовления: фальшфейеры белого, красного, желтого и зеленого огней, 30 мм и 40 мм реактивные сигнальные патроны, в том числе и однозвездные парашютные 26 мм сигнальные патроны цветного огня и цветного дыма.
Помимо тех изделий, о которых мы уже рассказали, существуют различные имитационные изделия и эффекты, которые были разработаны и испытаны на самых различных киносъемках, у самых разных киномастеров: режиссеров, операторов, художников, маститых и признанных мастеров других профессий киноработников. Среди разработок имеются как не очень сложные, наиболее часто используемые пиротехнические изделия, производство которых исчисляется тысячами штук, так и редко применяемые, но тем не менее крайне необходимые, такие как приспособление для пуска стрел, имитация облаков и т.д. К этим имитационным средствам относятся:
1. Имитационные пиротехнические средства, изготовление которых может осуществляться в пиротехнической мастерской киностудии или непосредственно на съемочной площадке, перед съемкой (на натуре и в павильонах), — имитаторы взрыва мин, гранат и артиллерийских снарядов; способ подъема пламени на значительную высоту; имитация горящей расплавленной смолы, горения разлившихся по воде нефтепродуктов; стрельбы из автоматического стрелкового оружия; артиллерийского выстрела; расплавленного металла, взрывания различной техники и нефтепродуктов, эффекта электросварки, искр при пожаре, а также шашки для имитации горения самолета при комбинированных съемках; приспособления для изготовления крутящегося пушечного ядра; пневматического устройства для осуществления имитации попадания пуль; получение эффекта «холодного» малодымного пламени; керосиновые и нафталиновые фугасы (ФОГи — Фугас Огненный); имитаторов разрыва зенитных снарядов различного калибра; оформления эффекта попадания пули в лицо человека; осуществление эффекта попадания артиллерийского снаряда в любое место декораций.
2. Помимо использования собственных разработок широко применяются промышленные и оборонные учебные имитационные пиротехнические средства; имитаторы взрыва (ИМы) различного калибра пушек; имитаторы попадания пуль (ИПП); электрозапалы и электродетонаторы пониженной мощности для оформления эффекта попадания пуль и осколков на тело человека, на костюм человека с последующим появлением крови, и другие средства.
Данной книгой предусмотрено знакомство с технологиями. изготовления различных фейерверочных средств и изделий: «люсткугелей»; «бураков», с двумя типами искристых фонтанов; «китайских колес» и других изделий. При их разработке учитывались самые благоприятные обстоятельства и параметры для проведения фейерверков: высота подъема изделий, время «работы», светимость, фейерверочный эффект, размер элементов и фигур, ограниченность пространства кинокадра и т.п.
К этой группе пиротехнических средств относятся служебные изделия и вспомогательные материалы.
Одни из них могут и должны изготавливаться в условиях пиротехнической мастерской или цеха при киностудии: «стопин» или «нить стопина»; звездки цветных огней и «швермеры» — для дальнейшего снаряжения изделий; различные кле- $ евые растворы; картонные и бумажные гильзы различного калибра и назначения, фитили и другие.
Вспомогательные средства воспламенения и взрывания промышленного производства, которые в силу их стандартизации, трудоемкости, точности и других параметров нет смысла делать кустарным способом: различные электровоспламенители, большой, но еще недостаточный ассортимент электродетонаторов, шнур огнепроводный; шнур детонирующий, спички «ветровые», спички «охотничьи» и др.
Большое разнообразие задач, порой неожиданных, решение которых требует дымовых и других пиротехнических средств, и ограниченный ассортимент промышленного изготовления поставили перед пиротехниками задачу разработки технологий изготовления своими силами и средствами различных дымовых и других изделий и эффектов в условиях, мягко говоря, далеко не идеальных, в пиротехнических мастерских при киностудиях. К чести кинопиротехников надо сказать, что со многими задачами они справились хорошо. Другие вопросы, другие изделия еще надо разрабатывать, надо готовить для них не только теоретическую, но и практическую основу, базу. Задерживает решение таких задач недостаточное количество и качество материалов, химикатов, пригодных в наших специфических, кинематографических условиях работы. Много нерешенных задач и в фейерверочном искусстве, где очень большое поле деятельности для поисков, проб и много работы. Скоро мы перейдем к изложению технологических процессов изготовления различных дымовых средств и других пиротехнических изделий в условиях наших мастерских, поговорим и о промышленных пиротехнических изделиях, об их положительных и отрицательных свойствах и характеристиках, о том, как легче и дешевле изготовить те или другие пиротехнические средства с соблюдением правил техники безопасности, с наименьшим нанесением вреда окружающей среде. Но не забудьте главного! Главным для нас вопросом и главной задачей всегда будет наибольший визуальный эффект.
Часто молодые люди, называясь пиротехниками театра, клуба, цирка, спрашивают рецепт того или иного пиротехнического изделия; спрашивают многие наши рецепты маститые пиротехники из зарубежных стран (что уж тут говорить о пиротехниках с периферийных студий). И тогда поло-жение становится крайне щекотливым. Почему? Объясню, дело в том, что у каждого пиротехника есть (должна быть!) записная книжка, куда заносятся рецепты, заметки и замечания для проверки, а также проверенные рецепты (чаще всего эта книжка хранится или в шкафу раздевалки, или -дома, но бывает и в кармане, с собой). Но, как таковой, рецепт «коллеге» дать невозможно. И не потому, что «секрет фирмы», мол, я знаю, я умею, я сделаю, а ты — как хочешь. Нет. Совсем не так. Очень многие рецепты, особенно редких по применению и сложных пиротехнических изделий, сами по себе — ничего не дадут. Допустим, что будет у такого «пиротехника» рецепт, вернее, список химикатов смеси и их процентное соотношение в ней. Только не всегда можно сделать пиротехническое изделие по такому рецепту. Можно сделать лишь некоторые составы, где два-три знакомых компонента, в основном нейтральных, подвергаются механическому соединению и смешиванию. И даже эти смеси по рецептам надо знать: что смешать в первую очередь, а что можно ввести потом. Большинство пиротехнических изделий или эффектов, помимо списка химикатов, потребных для их изготовления и их процентного содержания, требуют не ТОЛЬКО твердых, знаний технологического процесса, но и неукоснительного его соблюдения. '
Именно технологический процесс изготовления сложного пиротехнического изделия порой останавливает нас от передачи рецепта другому лицу, «коллеге».
Представим себе, что один из нас, зная рецепт получения гремучей ртути, но не зная технологии ее изготовления или получения, передал его просящему. При возможности или надобности тот начинает на свой страх и риск изготавливать это зелье, не зная технологии, не зная безопасных количеств, не соблюдая мер безопасности по всей цепочке изготовления — от грязной посуды, до работы без противогаза. К чему приведет такая пиротехническая самодеятельность? Двух мнений быть не может: приведет это рано или поздно к несчастному, трагическому случаю. А когда будет вестись расследование (обязательное!) несчастного случая — выяснится, что рецепт пострадавший узнал, переписал у дяди Васи, дяди Коли с «Мосфильма», с-«Ленфильма», со студии им. Довженко. И дело не в том, что надо бояться ответственности, хотя это тоже немаловажно, но главное — пострадает человек, станет калекой.
Разработка и выпуск «Технологических записок оружейно-пиротехнического цеха киностудии «Мосфильм» и приказ по Госкино об обязательном соблюдении требований при изготовлении пиротехнической продукции намного облегчили и работу кинопиротехников, и их взаимоотношения с творческими группами, техническими службами киностудий. «Технологические записки» — это обобщение опыта большого, грамотного и опытнейшего коллектива, в котором каждый сотрудник'внес свою лепту, исходя из своих сил и возможностей. При написании данной книги «Пиротехник. Искусство изготовления фейерверков» я руководствовался основными положениями указанных «Технологических записок». При этом надеюсь, что работа творческая и изыскательская по новым рецептам, с новыми химикатами не прекратится и даже не ограничится. Скорее, наоборот. Процесс обновления старых рецептов, процесс искания и проб новых химикатов, новых пиротехнических изделий и эффектов не остановить никогда. Он (этот процесс) будет продолжаться всегда, пока будет нужна профессия пиротехника, пока будет нужно фейерверочное искусство. Только процесс этот должен идти от теоретических разработок, с применением данных лабораторных работ, с изучением всех свойств и характеристик новых химикатов и их рекомендаций по внедрению в пиротехническое производство. Только теоретически обоснованные количества различных химикатов можно допускать на опыты, на пробы, на хранение.
С сожалением приходится констатировать, что среди пиротехников очень мало людей ищущих и пытливых, стремящихся обновить старое, отыскать и обосновать новое. Бывает и по-другому — появляется в коллективе такой человек, а возможности попробовать свои задумки он не имеет. Повседневная текучая работа, съемки, командировки, необходимость выпускать продукцию, нехватка нужных материалов, инструмента, оборудования, чаще всего смазывают благие порывы и задуманное не реализуется. Проходит время — придуманное забывается, мы «обрастаем» ленью, и новое не
;«fr^aw»wati«wii^^ 11 fi і 11 н і кт wrawnr jiwrn.w«wu«yj айааяййюизя*^^ мйїнї ja.-j. wATmi» і іиижмймм^тйя. появляется. Счастье для всего коллектива, когда в его среде находится человек, который добровольно берет на себя изыскательскую работу; работу, не дающую моментального результата; работу, зачастую неблагодарную, вредную, грязную. Работу, в которой надо не только возиться с химикатами, но и постоянно следить за литературой, изысканием этой литературы по библиотекам, по частным лицам; работу, когда коллеги, не всегда понимающие своего товарища, с недоверием, а иногда и враждебно смотрят на «чудака».
Конечно, есть и другие общие вопросы у кажт дого коллектива пиротехнических цехов при киностудиях, стоят они наравне с производственными вопросами, но решаются уж очень медленно. Остро стоит, особенно в последние годы, вопрос со снабжением химикатами. Не менее важен и вопрос складирования, вернее, нехватки, недостаточности складских емкостей, помещений. На всех студиях, у всех пиротехников большие претензии к снабженцам и промышленности по вопросу нехватки детонаторов пониженной мощности. Наша промышленность их практически не выпускает, а потребность с каждым годом растет, растут и пожелания и потребности съемочных групп в эффектах, которые можно сделать лишь электродетонатором пониженной мощности и определенной конструкции. После каждого кинофестиваля, которых в мировом кино стало очень много, киноработники, к которым мы, пиротехники, не относимся, насмотревшись различных пиротехнических эффектов 6 чужих фильмах, требуют от нас повторения этих эффектов уже в своих. Так, после просмотра фильма «Крестный отец»
________ ПИРОТЕХНИК всем режиссерам потребовался эффект посадки пули на лице человека. Многие требовали сделать идущего горящего человека. Эффекты эти, конечно, очень эмоционально сильны. Но наши технические средства сильно отстают от подобных средств и изделий пиротехнических фирм западных кинопиротехников, да и оплата нашей работы далеко не соответствует западной.
Поэтому кто-то делает подобный эффект, на свой страх и риск, переделывая стандартное изделие и превращая его в суррогат, без гарантий, что будет эффект и без гарантий безопасности актера. А ведь для актера лицо — источник жизни, источник его существования. Поэтому пиротехник делает эффект идущего горящего человека, человека-факела, на себе. Возникает вопрос: рисковать актером — нельзя, а собой — можно? Таких и подобных вопросов много, а работы в направлении безопасности еще больше. Но не надо бояться работы. Надо больше пробовать, искать и сомневаться, и снова искать и пробовать. Только мы сами — пиротехники — сможем улучшить наши изделия, наши эффекты; никто, кроме «чудаков» из нашей среды, не принесет их нам на тарелочке.
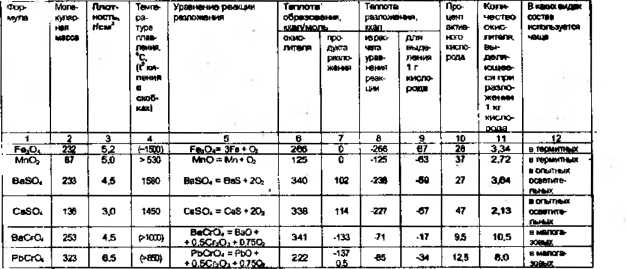
ВаСгО4 — хромат бария, хромовокислый барий, РЬСгО4 — хромат свинца, хромовокислый свинец.
149
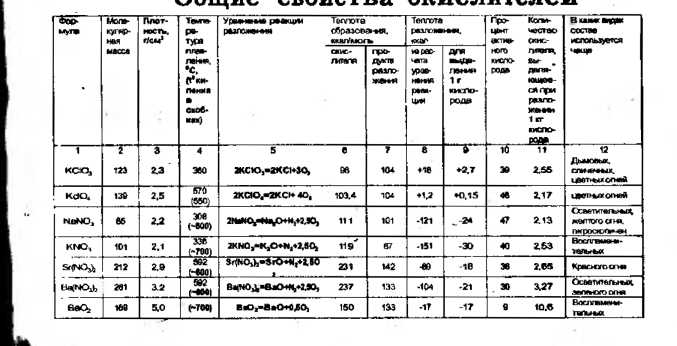
- ____________ПИРОТЕХНИК
Соли, для которых «гигроскопическая точка» меньше 78-80%, считаются гигроскопичными, и практическая работа с такими солями затруднена в пиротехнике. Насколько гигроскопична соль, можно судить о ее растворимости в воде — чем больше растворимость соли, тем она гигроскопичнее.
Приложение
Теплота
Атомная Оксид, образования, ккал
символ масса, А формула мол. масса q1= q
В пиротехнике еще мало используются: карбиды — соединения неорганических горючих с углеродом; сульфиды (за исключением Sb2S5 — сурьмы трехсернистой) — соединения тех же горючих с серой; фосфиды — соединения тех же горючих с фосфором. Особенно в пиротехнике кино, где лабораторная работа ведется слабо, да и то только в последнее время, где пиротехники, отработавшие со многими химикатами, даже не видели их ни разу. Конечно, в таких условиях трудно ожидать появления новых изделий и внедрения новых Химикатов и материалов. В конце концов, есть НИИ ПХ, лаборатории оборонных химических заводов, они то в курсе всех новинок в пиротехническо-фейерверочном вопросе. Пускай скажут свое научное слово. Новое слово. Полезное.
-757-